抗体医薬品の基本がわかる!作り方や作用機序などを丁寧に解説

今回はバイオ医薬品の中でも承認品目数の多い抗体医薬品について解説します。
目次
1.抗体とは?
抗体は生体内に細菌やウイルスが侵入した際に、攻撃し排除するために体内で作られる「免疫グロブリン」と呼ばれるタンパク質です。免疫細胞のうちB細胞が生産し、特異的な抗原と各々の抗体が結合し抗原分子の活性の阻害や細胞傷害活性を誘導します。
抗体の基本構造としては、図1(a)のように2本のH鎖(Heavy Chain)、L鎖(Light Chain)がジスルフィド結合した形となります。H鎖、L鎖には定常領域 (Constant region)と可変領域(Variable region)とがあり、定常領域が一定のアミノ酸配列を持つのに対し、可変領域は相補性決定領域 (Complementarity determining region:CDR)があり、アミノ酸配列の多様性に富み、抗原に対する特異性を決定する部位になります。
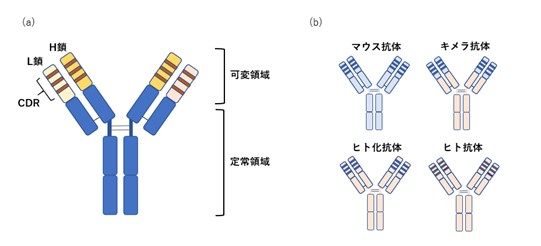
[図1:抗体の基本構造]
2.抗体作製方法(抗体医薬品の作り方)
抗体医薬品としては、単一の抗体産生細胞に由来するクローンから得られた「モノクローナル抗体」が中心になります。
モノクローナル抗体には図1(b)のようにマウス抗体、キメラ抗体、ヒト化抗体、ヒト抗体の4種類ありますが、承認されている抗体医薬品は主にヒト化抗体、ヒト抗体になります。
モノクローナル抗体の作製方法としては、以下のような方法があります。
(1)ハイブリドーマ法
マウスに抗原を投与すると体内でB細胞により抗体が産生されます。抗体を産生するB細胞と骨髄腫由来の無限に増殖する能力を持つミエローマ細胞を融合した「ハイブリドーマ細胞」からモノクローナル抗体を作製する方法です。
産生される抗体はマウス抗体ですが、マウス抗体は異種抗原のためヒトに投与すると抗体ができてしまうという問題から、免疫グロブリンの可変領域以外をヒト免疫グロブリンに置き換えたキメラ抗体、CDR以外をヒト免疫グロブリンに置き換えたヒト化抗体、マウス由来部分がないヒト抗体として改良されています。
キメラ抗体はマウスハイブリドーマ細胞からマウス抗体をコードする遺伝子をクローニングし、クローニングしたマウス由来可変領域遺伝子をヒト由来の定常領域遺伝子に連結させ、発現ベクターに挿入し、微生物や動物細胞などの宿主細胞で培養させ抗体を産生させます。
ヒト化抗体はCDRグラフト技術を用いて、マウス抗体のCDRとヒト抗体可変領域のフレームワーク領域からなる可変領域遺伝子を作製し、ヒト定常領域と連結させ挿入した発現ベクターを同様に培養細胞に導入し抗体を産生させます。
(2)ファージディスプレイ法
バクテリアに感染するバクテリオファージの表面に抗体フラグメントを提示させます。これらのファージを標的分子と反応させ、標的に結合したファージだけを選択的に回収します。その後、回収したファージを大腸菌に感染させることで複製・増殖させる「パニング操作」を繰り返し、標的分子に特異的に結合する抗体を取得します。得られた抗体フラグメントの配列を解析することで、完全ヒト型の抗体を作製することが可能です。
(3)ヒト抗体作製用トランスジェニックマウス法
内因性 Ig のノックアウトマウスにヒトIg 遺伝子を導入し、マウス抗体の代わりにヒト抗体が産生することができ、完全ヒト抗体を作製することができます。
(4)単一B細胞抗体クローニング法
感染症などの患者から標的抗原を用いて、抗原を特異的に認識する抗体を発現するB細胞を単離し、単一細胞から抗体遺伝子をクローニング、発現ベクターを動物細胞に導入して抗体を発現させてスクリーニングし、目的の抗体遺伝子をクローニングする方法です。
3.抗体医薬品の作用機序
抗体は図2のように標的分子との結合により作用します。
標的分子の受容体に抗体が結合することで受容体とリガンドの結合が阻害されシグナル伝達が阻害されます。
抗体がリガンドに結合することでも同様のシグナル伝達阻害がおこります。
また、受容体に抗体が結合することで、シグナル伝達を促進しアゴニストとして機能する抗体もあります。
標的分子に抗体が結合するとNK細胞などのエフェクター細胞が抗体に結合して、エフェクター細胞が標的細胞を攻撃する抗体依存性細胞傷害活性(ADCC:antibody dependent cellular cytotoxicity)をおこします。
同様に標的分子に抗体が結合すると補体系が活性化し、抗体が補体と結合して標的細胞を傷害する補体依存性細胞傷害活性(CDC:complement dependent cytotoxicity)をおこします。
また、抗体と薬物を結合させた抗体薬物複合体(ADC:antibody drug conjugate)は抗体を標的への作用剤ターゲッティングとして利用し、細胞内に取り込まれ薬物の作用を発揮します。
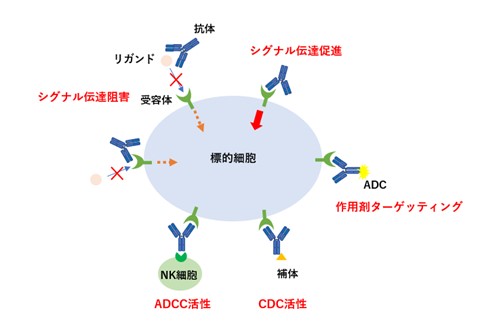
[図2:抗体医薬品の作用機序]
4.がん治療における抗体医薬品
承認されている抗体医薬品はがん治療、免疫系疾患、感染症や高脂血症など多くの疾患に用いられていますが、ここではがんを対象とした抗体医薬品の一部について説明します。
(1)免疫チェックポイント阻害抗体
免疫システムには免疫応答を活性化と抑制化する機構があり、抑制化としては自己細胞への過剰な免疫応答を抑制する免疫チェックポイント分子が存在します。
免疫チェックポイント分子として、PD-L1/PD-1経路が知られていますが、図3(a)のような腫瘍環境では腫瘍細胞が免疫系からの攻撃を避けるために利用されます。
細胞傷害性T細胞が腫瘍細胞への攻撃を続けると腫瘍細胞に発現するPD-L1受容体が、T細胞の表面に発現するPD-1に結合すると、T細胞の活性が抑制されます。
そのため、PD-L1/PD-1免疫チェックポイントを標的とした抗PD-1抗体や抗PD-L1抗体が開発されています。
抗PD-1抗体は「ニボルマブ」(オプジーボ)として知られており、PD-1に結合することでPD-L1とPD-1の結合を阻害し、T細胞を再活性化することができます。
(2)T細胞エンゲージャー抗体
B細胞の抗原CD19に結合する抗体と、T細胞受容体複合体CD3に結合する抗体の抗原認識部位を結合させた、二重特異性T細胞誘導(bispecific T-cell engager:BiTE)抗体が開発されています。
抗体可変領域のH鎖とL鎖をリンカーで結合した一本鎖抗体(single chain variable fragment:scFv)が用いられ、CD19特異的 scFvとCD3特異的 scFvがリンカーで連結した構造となっており、図3(b)のようにBiTE抗体によって患者自体のCD3⁺T細胞が標的のCD19⁺腫瘍細胞と架橋されCD3⁺T細胞が活性化することで標的腫瘍細胞を攻撃します。
抗CD19/抗CD3抗体は「ブリナツモマブ」として知られており、再発または難治性B細胞性急性リンパ性白血病の治療薬として承認されています。
さらに抗原特異性部位を増やした多重特異性抗体(マルチスペシフィック抗体)の開発も進められています。

[図3:がん細胞を標的とした抗体医薬品]
5.COVID-19と抗体医薬品
抗体医薬品は、新型感染症への対応にも大きな役割を果たしてきました。たとえば、新型コロナウイルス感染症(COVID-19)の世界的な流行時には、ウイルスのスパイクタンパク質など特定の抗原を標的とした中和抗体医薬品が迅速に開発され、大きな注目を集めました。これらの抗体医薬品は、ウイルスの細胞侵入を阻止することによって、感染拡大や重症化のリスクを低減する目的で使用されました。
こうした開発例は、抗体医薬品の柔軟性と即応性を示すものであり、将来的な感染症対策やパンデミック時の治療戦略においても重要なモデルとなります。
以上、今回は抗体医薬品の基礎知識について解説しました。
抗体医薬品は、その高い特異性と多様な作用メカニズムを活かし、がんや自己免疫疾患、感染症など幅広い疾患領域で活用されています。近年では抗体の構造や機能を最適化する技術が進展し、次世代型の抗体も注目を集めています。今後、より高機能で安全な抗体医薬を実現するための技術開発がますます期待されます。
[※関連記事:抗体医薬の高機能化技術の解説 はこちら]
(日本アイアール株式会社 特許調査部 N・Y)












](https://engineer-education.com/wp/wp-content/uploads/2024/01/crushing-150x150.png)



























