質量分析器を用いた分析(主な種類と原理):GC-MS/LC-MS/ICP-MS/GD-MS/SIMS《機器分析のキホン⑦》

1. 質量分析器を用いた主な分析方法(種類と概要)
質量分析器(質量分析装置、質量分析計)は、イオン化部、質量分離部、検出部からなっています。
帯電した粒子(イオン)は電場によって加速され、さらに運動するイオンは、電場、磁場によって曲げられますが、加速され方、曲げられ方はいずれも質量数を荷電数でわったもの(質量/電荷=m/z)に依存します。
そこで、イオン化部で帯電させ、気相に存在させた粒子を、質量分離部で種々の方法で分離し、検出することで、元素(分子)を特定します。代表的な質量分離部を表1にまとめます。
![代表的な質量分離部(二重収束型[FB]、四重極型[Q]、飛行時間型[TOF])](https://engineer-education.com/wp/wp-content/uploads/2023/11/instrumental-analysis_07_01.png)
【表1 質量分析器に用いられる代表的な質量分離部】
質量分析法(MS: Mass Spectrometry)には、目的元素(分子)を分離、イオン化する方法に応じて、次のようなものがあります。
[※関連記事:【分析化学を学ぶ】質量分析法とは?イオン化法の種類など要点解説 はこちら]
(1)クロマトグラフィー質量分析法(GC-MS、LC-MS)
- ガスクロマトグラフィー質量分析法(GC-MS: Gas Chromatography MS)
- 液体クロマトグラフィー質量分析法(LC-MS: Liquid Chromatography MS)
「クロマトグラフィー」とは、気体(GC)、液体(LC)などの流体を移動相として管(カラム)の中に保持された固定相と物質の相互作用によって混合物を分離、検出する分析法です。
[※関連記事:ガスクロマトグラフ質量分析(GC-MS)の基礎知識・要点解説 ]
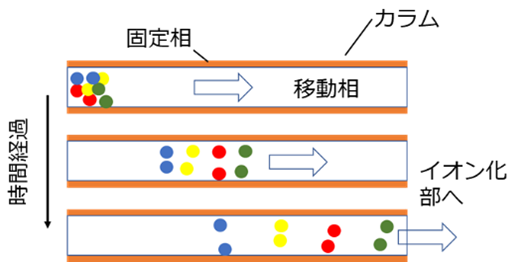
【図1 クロマトグラフィーの原理】
固定相との相互作用が強い成分はカラムを抜けるのに時間がかかり、弱い成分は短時間で抜けてきますので、カラムで分離された分子をイオン化し、質量分析器にかければ、分子の質量情報が得られます。
(2)誘導結合プラズマ質量分析法(ICP-MS)
誘導結合プラズマ質量分析法(ICP-MS: Inductively Coupled Plasma MS)は、アルゴンプラズマの中に溶液を霧化して導入し、溶液成分をイオン化して、質量分離部に送ります。
アルゴンプラズマは、アルゴンガスを流したトーチ管の先端にワークコイルを置き、コイルに高周波電流を流すことで作られる電磁場によってアルゴンを電離させて生成します(誘導結合プラズマ)。
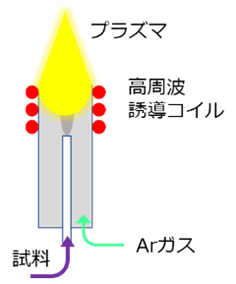
【図2 プラズマトーチ】
ICPでのイオン化率は、多くの元素で90%以上であり、イオン源としては理想的です。
GC、LC、ICP や、次に説明するGDは、もともと、分離した元素あるいは分子を、元素、分子に特有の吸光や発光によって特定していましたが、四重極型などの質量分析器が手軽に利用できるようになったことから、質量分析法への移行が進んでいます。
(3)グロー放電質量分析法(GD-MS)
グロー放電質量分析法(GD-MS: Glow Discharge MS)では、Arガス雰囲気下で固体試料をマイナス極としてグロー放電を行い、Arイオンでスパッタされて飛び出した試料構成元素をArプラズマ中でイオン化します。
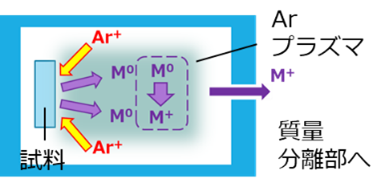
【図3 グロー放電質量分析法】
(4)二次イオン質量分析法(SIMS)
真空中で一次イオン(O、Cs等)を試料表面に照射すると、表面近傍の原子の一部がイオン(二次イオン)として飛び出してきます。
二次イオン質量分析法(SIMS: Secondary Ion MS)は、感度の良いTOF(Time-of-Flight)型の質量分離部を使い、パルス状一次イオン(Bi等)の照射量を少なくすれば(TOF-SIMS)、最表面を高感度で分析したり、分子状態を保ったままのイオンとして分析することもできます。
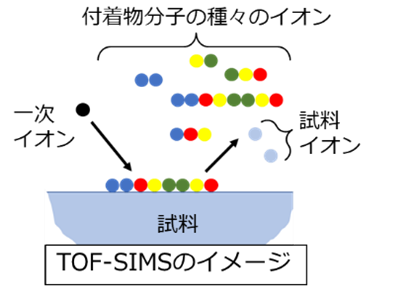
【図4 二次イオン質量分析法】
GD-MS、SIMSともに、深さ方向分析が可能です。
2.終わりに:機器分析は”結果を鵜呑みにしない姿勢”が重要
当連載では7回にわたって機器分析の基礎を紹介してきました。
機器分析は、一般に測定の自動化が容易であり、測定者の技量に依存しにくいため測定結果のバラつきが小さい、多元素の同時検出が可能なため迅速性にすぐれる、微量、微小領域の分析が比較的容易であるなどの利点があります。また、近年の機器分析技術の進歩はとても速く、いくつかの装置を組み合わせた複合装置も開発され多様な分析が可能になっています。
一方で、測定そのものがブラックボックス化しやすく、得られた結果を鵜吞みにして、間違った解釈に気づかないという弊害も出てきます。
ですから、分析を担当する方はもちろん、分析を依頼する立場の皆さんも、その答えで論理的な矛盾はないか、他に確認する方法はないか、など慎重に対応する必要があります。
ぜひ、分析結果をやみくもに信じることなく、クロスチェックを必ず行うという習慣も身に着けてください。
(アイアール技術者教育研究所 H・N)
- 第1回: 「機器分析」とは?「化学分析」との違いは?定性分析/定量分析など前提知識を解説
- 第2回: 非破壊で定量的に知る方法:励起と検出の組合せと信号の解釈
- 第3回: 分析対象の測定場所の絞り込み方法、形状・構造を知る方法
- 第4回: 電子顕微鏡(TEM,SEM)と走査プローブ顕微鏡(SPM)
- 第5回: 組成を知る:固体表面の分析方法(AES/EPMA/XPS/XRF)
- 第6回: 結晶構造を知る:XRD|分子構造を知る:FT-IR, Raman, NMR
- 第7回: 質量分析器を用いた分析(主な種類と原理):GC-MS/LC-MS/ICP-MS/GD-MS/SIMS