カルノーサイクルと逆カルノーサイクルの仕組みと熱効率 [熱力学の基礎④]

今回の連載コラムは、熱機関や冷凍機などで行われる作動流体のサイクルについて解説します。
1.熱力学における「サイクル」
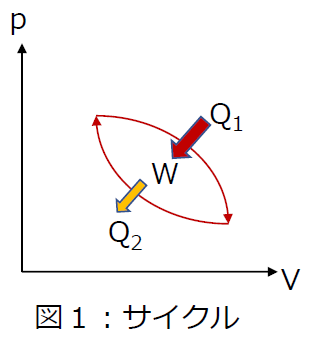
図1のように、作動流体がある経路を通って状態変化し、違う経路をたどって元の状態へ戻るとき、状態変化の経路は閉曲線となります。この変化を繰り返す連続的な循環を「サイクル」といいます。
熱力学の第二法則によれば、熱機関は高温熱源から熱量Q1を受け取り、外界へ仕事Wをなし、残りの熱量Q2を低温熱源へ放出します。(※熱力学の第一法則と第二法則に関する解説記事はこちら)
仕事Wが大きいほど熱の有効利用率が高い、つまり効率が良いことになります。
サイクルの熱効率 η=W/Q=(Q1-Q2)/Q1=1-(Q2/Q1) ・・・(1)
また図1において閉曲線の上側は、熱源から熱をもらって膨張する過程、下側は圧縮して外部へ仕事をするとともに、低温熱源へ熱を捨てる過程を示します。
したがって、閉曲線で囲まれた面積は1サイクルで行われる有効な仕事量Wを表しています。
閉曲線で囲まれる面積が大きいほど、熱機関の熱効率が大きく、工業的に有用であることを示します。
2.カルノーサイクルとは
フランスの物理学者カルノー(Nicolas Léonard Sadi Carnot)は、熱機関の研究を行い1824年、図2(a)に示すような等温変化と断熱変化で構成されることで、熱効率が最大となる理想的なサイクルが得られることを示しました。
「カルノーサイクル」 (Carnot Cycle)とは、理想気体を動作流体とし、次の4工程からなる可逆サイクルです。
(※可逆変化は現実には存在しませんが、熱力学では一般に、可逆変化を仮定して状態変化を考えます。)
- 等温膨張(図2の①→②):高熱源温度T1一定で、この間に熱量Q1を受け取る
- 断熱膨張(図2の②→③):膨張して外部へ仕事をなし、温度が低下する
- 等温圧縮(図2の③→④):低熱源温度T2一定で、この間に熱量Q2を捨てる
- 断熱圧縮(図2の④→①):圧縮して温度が上昇し、①の状態に戻る
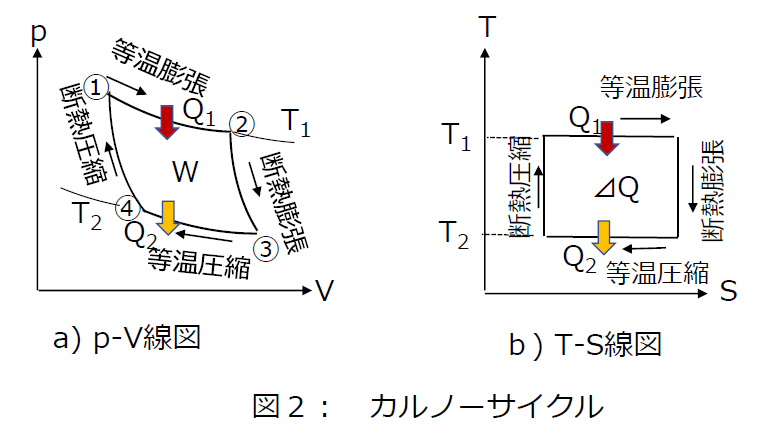
(※p-V線図の解説は、当連載の前回の記事「《気体の状態変化を理解》理想気体の状態方程式、熱容量と比熱などを解説」をご参照ください。)
等温変化と断熱変化からなるカルノーサイクルでは、熱量Qと温度Tの間に次の関係が成り立ちます。
Q2/Q1=T2/T1 ・・・(2)
したがって(1)、(2)式より、カルノーサイクルの熱効率ηcは
ηc=1-(T2/T1) ・・・(3)
となります。
カルノーサイクルの熱効率は、高温低温熱源の温度だけで決まります。
なお、完全な断熱や、温度一定など、カルノーサイクル成立条件の実現は困難であり、実際にカルノーサイクルを用いた熱機関を製作することはできません。あくまで実用的サイクルの効率を比較する際の基準として用いられます。
3.逆カルノーサイクルとは
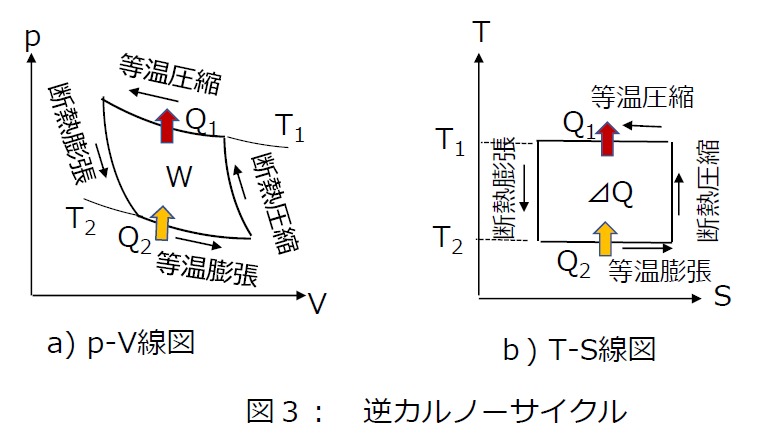
「逆カルノーサイクル」(カルノー冷凍サイクル)とは、冷凍機やヒートポンプ、エアコンの理想サイクルで、図3(a)のようにカルノーサイクルを逆方向に作動させるものです。
逆サイクルなので、外部へ仕事をする代わりに、外部から仕事をもらって、等温膨張する際に低温熱源から熱を受け取り、等温圧縮する際に高温熱源へ熱を放出することができます。作動流体(冷媒)が膨張する際に、シリンダ内部の温度が低温熱源より低下するので熱を取り込むことができます。このサイクルを回すために外部から与える仕事が消費動力(消費電力)ということになります。
性能指標については、熱効率ではなく「成績係数(COP)」を用います。COPは消費動力に対してどのくらいの冷房能力あるいは暖房能力を発揮できるか、つまりどのくらいの熱を取り込むことができるかを示すもので、効率と違って1より大きな数字となります。
[※関連記事:冷凍機の種類と仕組み、性能の考え方 ]
4.熱力学線図(T-S線図)で表す
「p-V線図」のように、2つの状態量で気体の状態を定めることができます。
2つの状態量としてp-V線図の他にいくつかの熱力学線図があります。
温度Tを縦軸に、エントロピーSを横軸にとった「T-S線図」や、圧力pを縦軸に、エンタルピーHを横軸にとった「p-H線図」などがあります。
熱力学線図は、冷凍機などの設計や運転において、サイクルを循環する冷媒の状態変化や、熱や仕事の出入りを知るために使用されます。
熱力学の第一法則と第二法則に関する解説記事でもご紹介していますが、エントロピーの式はdS=dQ/Tですから、熱の出入りの無い断熱変化は等エントロピー変化です。
したがって、カルノーサイクルと逆カルノーサイクルをT-S線図で表すと、図2,3(b)のように長方形となります。また、T-S線図で表したサイクル曲線で囲まれた面積は外部から受け取った熱量を示します。
次回は、熱伝導・熱伝達・放射という「伝熱3形態」の重要ポイントを解説します。
(日本アイアール株式会社 特許調査部 S・Y)
- 第1回: 《熱力学初心者向け》熱と仕事、エネルギーの関係など必須前提知識を押さえよう
- 第2回: 熱力学の第一法則と第二法則を理解する
- 第3回: 《気体の状態変化を理解》理想気体の状態方程式、熱容量と比熱などを解説
- 第4回: カルノーサイクルと逆カルノーサイクルの仕組みと熱効率
- 第5回: 伝熱3形態の重要ポイントを厳選解説 (熱伝導/熱伝達/放射)
- 社会人のための熱力学 [※社会人のための機械工学シリーズ 第2回](講師:技術士 近藤孝邦 氏)