医療機器に関する承認審査と申請書・添付資料(STED)の作成【提携セミナー】
おすすめのセミナー情報
もっと見る| 開催日時 | 2021/8/27(金) 10:30~16:30 |
|---|---|
| 担当講師 | 大室 欣一 氏 |
| 開催場所 | Zoomによるオンラインセミナー |
| 定員 | - |
| 受講費 | 【オンラインセミナー(見逃し視聴なし)】:47,300円 【オンラインセミナー(見逃し視聴あり)】:52,800円 |
「承認審査や認証審査の流れや種類などを把握したい!」
「申請書の書き方やSTEDの作成方法を詳しく理解したい!」
という方におすすめのセミナー。
保険適用等も含めて詳しく学習できます!!
医療機器に関する
承認審査と申請書・添付資料(STED)の作成
《承認申請書や認証申請書の書き方、STEDの作成方法を理解する》
【提携セミナー】
主催:株式会社情報機構
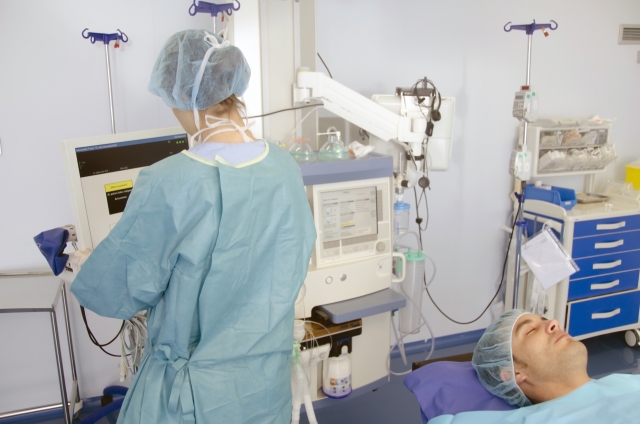
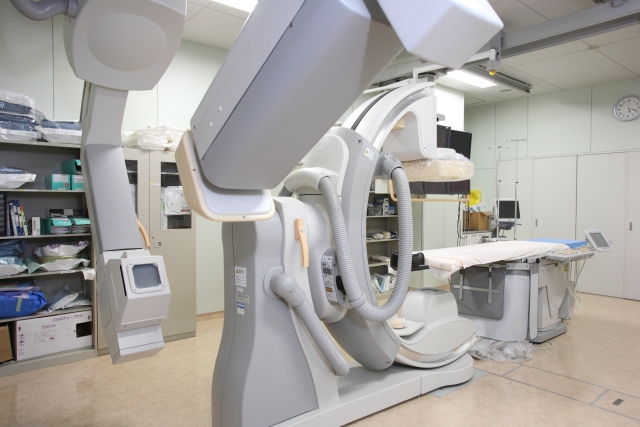
医療機器の承認審査制度は、製造承認と輸入承認という制度から、現在の製造販売承認及び製造販売認証制度に変わりました。我が国における医療機器の許認可制度の変遷と現在のシステムの概要、QMS・GVP制度との関連、適合性調査申請、申請の際に参照すべき厚労省・他省の通知及び国際・国内基準、申請に必要な情報などを紹介するとともに、Webサイトの画面や申請の具体例、 簡単な演習を交え、承認申請書や認証申請書、STEDの作成の実際を紹介します。生物学的安全性試験のガイドラインの改訂など、最新の医療機器の審査に関する通知についてもご説明する予定です。
初めて申請を行う方や、申請のコツを知りたい方に特におすすめの内容となっております。
◆ 受講後、習得できること
・医療機器の承認審査制度
・承認(認証)に必要な通知の知識
・ISO、IEC及びJISに関する知識
・申請書の作成の実際
・STED作成の実際
◆ 本テーマ関連法規・ガイドラインなど
・医薬品医療機器法
・ISO 10993、14971など
・IEC 60601-1、60601-1-2、62304など
・JIS (上記ISO、IECと対応するJISの国際規格との相違点)、及び他のJISなど
◆ 講演中のキーワード
・医療機器の承認
・医療機器の製造販売承認
・医療機器の製造販売認証
・医療機器の認証基準
・医療機器の承認基準
担当講師
大室 欣一 氏
セミナープログラム(予定)
・医療機器における承認審査
承認審査制度の変遷
現在の承認審査制度
医療機器の分類について
医療機器のクラス分類について
医療機器の製品群について
QMS適合性調査について
信頼性調査について
申請区分について
・承認審査の流れ
承認審査の流れ
認証審査の流れ
一部変更承認/認証について
軽微変更承認/認証について(一部変更との違いを含む)
一品目の範囲について
・審査ガイドラインの解説
承認基準
認証基準
ISO、IEC、及びJISなどの基準
厚労省通知/他省の関連通知
・治験について
治験が必要な場合
国内治験
外国治験
・書類作成及び申請
FD申請ソフトの利用
認証申請書
適合性調査申請書
適合性調査手数料計算ツール
・承認申請書の書き方
・認証申請書の書き方
・添付資料(STED)の作成方法
・書き方の演習
能動医療機器
単回使用医療機器
STED
・保険適用について
保険適用の基礎
保険適用の厚生労働省への申請方法
・医療機器WEB申請プラットフォーム(DWAP)の操作方法
・再製造単回使用医療機器の製造販売承認申請について
・最新の医薬品医療機器法、省令の改正について
・最近発出された通知について
質疑応答
公開セミナーの次回開催予定
開催日
2021年8月27日(金) 10:30-16:30
開催場所
【Live受講】 Live配信セミナー(リアルタイム配信) ※会社・自宅にいながら学習可能です※
オンライン配信のご案内
★ Zoomによるオンライン配信
★ 見逃し視聴
については、こちらをご参照ください
受講料
- 【オンラインセミナー(見逃し視聴なし)】:1名47,300円(税込(消費税10%)、資料付)
*1社2名以上同時申込の場合、1名につき36,300円
- 【オンラインセミナー(見逃し視聴あり)】:1名52,800円(税込(消費税10%)、資料付)
*1社2名以上同時申込の場合、1名につき41,800円
*学校法人割引;学生、教員のご参加は受講料50%割引
配布資料
- 配布資料はPDF等のデータで送付予定です。受取方法はメールでご案内致します。
(開催1週前~前日までには送付致します)。
*準備の都合上、開催1営業日前の12:00までにお申し込みをお願い致します。
(土、日、祝日は営業日としてカウント致しません。)
備考
- 当日、可能な範囲で質疑応答も対応致します。
(全ての質問にお答えできない可能性もございますので、予めご容赦ください。) - 本講座で使用する資料や配信動画は著作物であり、無断での録音・録画・複写・転載・配布・上映・販売等を禁止致します。
お申し込み方法
★下のセミナー参加申込ボタンより、必要事項をご記入の上お申し込みください。
★【オンラインセミナー(見逃し視聴なし)】、【オンラインセミナー(見逃し視聴あり)】のいずれかから、ご希望される受講形態をメッセージ欄に明記してください。