3分でわかる 希土類金属(レアアース)の基礎知識・要点解説

希土類金属(レアアース)は、電気自動車(EV)、再生可能エネルギー、通信機器、そして軍事技術に至るまで、現代の最先端産業に欠かせない素材です。希土類金属は、地殻中に極端に少ない元素ばかりではありませんが、経済的に採掘・分離できる鉱床が限られ、精製も難しいことから、供給上の重要性が高い元素群です。その特異な物理化学的性質から「産業のビタミン」とも呼ばれます。
本シリーズの記事では、レアアースの基礎から、その電子構造に由来する特徴的な磁気特性や発光特性に至るまでを解説します。
目次
1.希土類金属(レアアース)とは?
高付加価値産業を支える希土類金属(レアアース、または稀土類元素、rare earth elements:REE)は、その供給懸念の高まりを背景に、世界的に注目されています。
レアアースとは単一の金属を指す言葉ではなく、スカンジウム(Sc、原子番号21)、イットリウム(Y、原子番号39)、およびランタノイドの15元素を合わせた計17元素の総称です(図1、表1)。
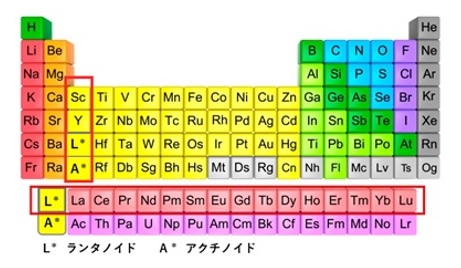
【図1 元素周期表中の希土類金属の位置】
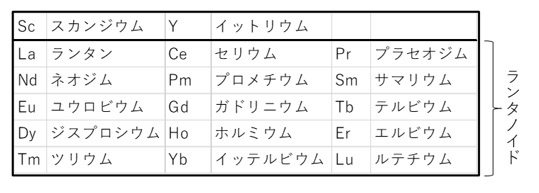
【表1 希土類金属の元素記号と和名】
2.実務上の分類
実務においては、イオン半径の大きさと分離の難易度に基づき、大きく2つに分けられます。
- 軽希土類(LREE): La, Ce, Pr, Nd, Smなど。比較的埋蔵量が多く、ネオジム磁石などの高性能永久磁石や触媒などに使われます。
- 重希土類 (HREE): Dy, Tb, Ho, Er, Yb, Luなど。希少価値が極めて高く、ハイテク産業の性能を左右する「鍵」となります。
ただし、Sm、Eu、Gd、Tb、Dyなどの扱いは分野によって異なり、中希土類として区分される場合もあります。Yはランタノイドではありませんが、化学的挙動が重希土類に近いため、重希土類側に含めて扱われることがあります。
3.希土類金属の特異な性質とその理由
希土類金属(レアアース)が「産業のビタミン」と呼ばれる理由の一つは、鉄やアルミニウムといった一般的な金属と決定的に異なる「内側に隠れた4f軌道」に由来する特異な性質にあります。
ランタノイド元素の原子番号は57~71で、原子番号が増えるにつれて、主に内側の4f軌道に電子が順次入っていきます。最外殻には主に6s電子が存在し、一部の元素では5d電子も関与します。この内側の4f軌道が、希土類元素に特有の磁性や発光特性に深く関係しています。
通常、電子はエネルギー準位の低い軌道から順に入っていきますが、ランタノイドでは、最外殻ではなく内側の4f軌道に電子が順次充填されていく点が特徴です。その結果、磁性・光学特性という物理的な強みと、分離の難しさという化学的な課題を同時に生み出しています。
(1)強力な磁性と鋭い発光(物理的特性)
レアアースは、非常に強力な磁力を持つ永久磁石(ネオジム磁石など)や、鮮やかな発光体(LEDの蛍光体、レーザー光源)として利用されます。
【この特徴の背景:4f軌道と不対電子】
原子構造の内側にある「4f軌道」に、ペアにならない電子(不対電子)が最大7つ(例えば:Gd3+)まで入るためです。この不対電子が磁気モーメントを生み、強い磁性の起源となります。また、4f電子のエネルギー準位間の遷移により、鋭い発光スペクトルを示すことがあります。
(2)外部に影響されない安定性(4f遮蔽効果)
希土類元素に由来する発光や磁気特性は、熱や化学反応といった周囲の環境の影響を受けにくい場合があります。例えば、特定の希土類元素を添加することで、高温下での磁気特性や発光特性の安定性を高めることができます。
【この特徴の背景:4f軌道の遮蔽効果】
4f軌道がさらに外側の電子殻(5s、5pなど)によって物理的に「覆い隠されて(遮蔽されて)」いるため、外界からの干渉を受けにくい「原子本来の性質」を保つことが可能です。
(3)化学的類似性と分離の困難さ
17種類のレアアースは、化学的な性質(反応のしやすさなど)が驚くほど似通っています。そのため、異なる元素が混ざり合って存在し、それらを1つずつ分ける「分離・精製」が極めて困難です。
【この特徴の背景:3価イオンの安定性とイオン半径の近さ】
多くの希土類元素は安定な3価イオンを形成しやすく、イオン半径も互いに近いため、化学的な挙動がよく似ています。そのため、鉱石中で共存しやすく、個々の元素に分離することが難しくなります。
(4)ランタノイド収縮:分離を可能にする手がかり
元素周期表の一般的な傾向として、原子半径は同一周期内では左から右へ行くほど小さくなり、同じ族では上から下へ行くほど大きくなります。
一方、ランタノイド元素では、LaからLuへと原子番号が大きくなるにつれて、3価イオンの半径が徐々に小さくなります。例えば、表2に示す結晶半径ベースのM3+半径では、La3+の117 pmからLu3+の100 pmまで低下しています。この現象を「ランタノイド収縮」といいます(表2)。
ランタノイド収縮によって生じるわずかな「サイズの差」は、似た性質を持つ希土類元素を分離するうえで重要な手がかりとなります。
【この特徴の背景:ランタノイド収縮】
ランタノイド収縮は、4f電子による核電荷の遮蔽が不十分であることに起因します。
通常、内側の電子は外側の電子に対する原子核の引力を弱める働き、すなわち遮蔽効果を持ちます。しかし、ランタノイドでは、原子番号が増えるにつれて内部の4f軌道に電子が順次入っていきます。4f軌道は形状が複雑で、電子分布が空間的に分散している(比較的まばらである)ため、核電荷を遮蔽する力が比較的弱いとされています。そのため、原子番号が増えるにつれて有効核電荷が大きくなり、外側の電子が原子核側へ引き寄せられます。その結果、原子半径やイオン半径が徐々に小さくなります。
一般に、内部電子による遮蔽効果は、s軌道、p軌道、d軌道、f軌道の順に弱くなるとされます。
希土類イオンは比較的大きなイオン半径を持つため、錯体形成時には6配位から高配位数まで、さまざまな配位構造をとることがあります。
| 原子番号 | 元素記号 | 原子量 | 原子の電子配置 | M3+イオンの電子配置 | 原子価 | 原子半径(pm) | M3+半径(6配位)(pm) | M3+塩の水溶液の色 |
| 21 | Sc | 44.97 | 3d14s2 | 3d0 | +3 | 163 | 088 | 無色 |
| 39 | Y | 88.92 | 4d15s2 | 4d0 | +3 | 178 | 104 | 無色 |
| 57 | La | 138.92 | 5d16s2 | 4f0 | +3 | 187 | 117 | 無色 |
| 58 | Ce | 140.13 | 4f15d16s2 | 4f1 | +3, +4 | 183 | 115 | 無色 |
| 59 | Pr | 140.92 | 4f36s2 | 4f2 | +3, +4 | 182 | 113 | 緑 |
| 60 | Nd | 144.27 | 4f46s2 | 4f3 | +2, +3, +4 | 181 | 112 | 赤紫 |
| 61 | Pm | 147.00 | 4f56s2 | 4f4 | +3 | 180 | 111 | 淡赤 |
| 62 | Sm | 150.35 | 4f66s2 | 4f5 | +2, +3 | 179 | 110 | 淡黄 |
| 63 | Eu | 152.00 | 4f76s2 | 4f6 | +2, +3 | 198 | 109 | 無色 |
| 64 | Gd | 157.26 | 4f75d16s2 | 4f7 | +3 | 179 | 108 | 無色 |
| 65 | Tb | 158.93 | 4f96s2 | 4f8 | +3, +4 | 176 | 106 | 無色 |
| 66 | Dy | 162.51 | 4f106s2 | 4f9 | +2, +3, +4 | 175 | 105 | 黄 |
| 67 | Ho | 164.94 | 4f116s2 | 4f10 | +3 | 174 | 104 | 淡黄 |
| 68 | Er | 167.27 | 4f126s2 | 4f11 | +3 | 173 | 103 | 桃色 |
| 69 | Tm | 168.94 | 4f136s2 | 4f12 | +2, +3 | 172 | 102 | 淡緑 |
| 70 | Yb | 173.04 | 4f146s2 | 4f13 | +2, +3 | 194 | 101 | 無色 |
| 71 | Lu | 174.99 | 4f145d16s2 | 4f14 | +3 | 172 | 100 | 無色 |
【表2 希土類元素の電子配置、原子価及び半径と色】
※表中のM3+半径(6配位)は、結晶半径ベースの値です。有効イオン半径として示される値とは異なる場合がありますが、La3+からLu3+にかけてイオン半径が徐々に小さくなるというランタノイド収縮の傾向は共通しています。
4.希土類金属の分離・精製
先端材料として利用するには、性質の似たイオン同士を分ける必要があります。主に以下の3つの手法が用いられます。
- 沈殿法:溶解度の違いを利用して、結晶化や沈殿を繰り返して分離する方法です。
- イオン交換法:イオン交換樹脂を用い、キレート試薬などの溶離液を流して、樹脂との結合力の差(半径の差に由来)を利用して順次溶かし出します。
- 溶媒抽出法:水溶液と有機溶媒の間での溶解度の差を利用します。配位子と結合して錯体を形成させ、特定の金属イオンを有機溶媒相へ移すことで分離・精製します。
他に膜の利用法や沈殿抽出の組み合わせ法などもありますが、ここでは割愛します。
5.産業上の重要性と鋼の純化
レアアースはハイテク材料としてだけでなく、既存産業の強化にも使われます。
- 鋼(はがね)の純化
希土類元素は酸素や硫黄と結合しやすいため、溶鋼に添加することで不純物を除去(純化)できます。また、希土類元素は酸化物・硫化物などの介在物の形態や分布を制御し、組織の微細化や靭性・耐食性などの改善に寄与することがあります。 - 磁性体・発光材料などのハイテク材料
多くの希土類元素では、4f電子に由来する特有のエネルギー準位が形成されます。そのため、発光材料や磁性材料として、蓄電池、発光ダイオード、レーザー、永久磁石などの性能向上に重要な役割を果たしています。 - 幅広い応用
イオン半径や価数など、希土類元素特有の化学的性質を利用して、触媒、固体電解質、酸化物高温超伝導体、水素吸蔵合金などにも、広く使われています。
この部分は本シリーズの第2部と第3部で詳しく解説します。
6.世界の供給網と中国の現状
現在、中国は世界最大級のレアアース生産国であり、採掘・分離・精製の各段階で大きな影響力を持っています。その分布には「北軽南重」の特徴があります。
内モンゴル自治区包頭の軽希土類鉱床、四川省涼山の軽希土類鉱床、江西省贛州(かんしゅう)をはじめとする南方5省の中重希土類鉱床の三大生産拠点があります。
内モンゴル包頭のバヤンオボ鉄、ニオビウム、希土類共生鉱床は、希土類埋蔵量が世界最大であり、軽希土類が希土類鉱物の79%を占めます。
江西省贛州市は重希土類の製錬・分離の中心地として知られています。中国稀土集団が設立された2021年時点では、五鉱稀土や贛州稀土集団など、関連企業の拠点が置かれていました。
近年、中国では軽希土類を中心とする北方の拠点と、重希土類を中心とする南方の拠点を軸に、レアアース産業の集約が進んでいます。
(1)中国北方希土(集団)
中国北方希土(集団)(China North Rare Earth (Group))は、1961 年に設立され、前身は包頭鉄鋼希土類実験工場(Baotou Steel Rare Earth Experimental Plant)です。内モンゴル自治区包頭市希土類ハイテク産業開発区に位置し、バヤンオボ鉱床という資源面の強みと、希土類研究所などの研究開発基盤を背景に、主に軽希土類精鉱及び機能材料の生産と販売を行っています。
会社の製錬分離生産能力は120,000トン/年、希土類金属生産能力は10,000トン/年、希土類機能材料の磁性材料合金は41,000トン/年、研磨材生産能力は23,500トン/年、水素貯蔵合金は8,300トン/年、発光材料は100トン/年、希土類触媒は12,000立方メートル/年とされています。
(2)中国稀土集団
中国国有の希土類金属企業「中国稀土集団」は、2021年12月23日に設立されました。
国有資産監督管理委員会の下で運営され、五鉱稀土、中国稀有稀土股份有限公司、贛州稀土集団有限公司が傘下に入ります。
ということで今回は、希土類金属について知っておきたい基礎知識をご紹介しました。
次回は、希土類金属の磁性体への応用について解説します。
(日本アイアール株式会社 特許調査部 H・L)
《引用文献、参考文献》
- 塩川二朗,「希土類元素の物性とその応用」, 電気化学および工業物理化学 58 巻 (1990) 8 号
https://www.jstage.jst.go.jp/article/kogyobutsurikagaku/58/8/58_702/_pdf/-char/ja - N.E.Topp著,塩川二朗,足立吟也訳,希土類元素の化学,化学同人(1974)
- 加納剛,柳田博明,レア・アース,技報堂(1980)
- レア・アース(増補改訂版),新金属協会(1980)
- 塩川二朗監修,レア・アースの最新応用技術,シーエムシー(1985)
- 太田 充恒,「希土類元素って?」 産総研(Webサイト)
https://staff.aist.go.jp/a.ohta/japanese/study/REE_ex_bs.htm - 足立吟也,希土類の科学,化学同人(1999)
- 鈴木 康雄,希土類の話,裳華房(1998)
- 馬淵 久夫,元素の辞典,朝倉書店(1994)
- 太田 充恒,「マンガン団塊の希土類元素」,月刊海洋 号外25「現代海洋化学・II」(2001)
- 百度百科,企業概要ページ(中国のWEBサイト)
中国北方稀土(集团)高科技股份有限公司
中国稀土集团有限公司