《非臨床試験のルール》GLPの概要・早わかり解説

以前に掲載したコラム「GCPの概要・早わかり解説」では、治験のデータを倫理性・信頼性基準のもとで収集するルールである「GCP」(Good Clinical Practice)の基本的な知識をご紹介しました。
今回は、医薬品開発では治験の前段階の非臨床試験のルールである「GLP」の概要をご紹介します。
1.GLPとは?
「GLP」とは”Good Laboratory Practice“の略称で、安全性に関わる非臨床試験・前臨床試験の信頼性を確保するための基準です。
新規医薬品の開発において、安全性を正しく評価することが極めて重要ですが、スクリーニングを経た新薬候補物質の臨床試験に先立ち、ウサギやイヌなどを使った動物実験(in vivo)、あるいは細胞培養などの試験管内の実験(in vitro)により安全性・有効性に関する試験(非臨床・前臨床試験)が行われます。
前臨床試験データを作成するにあたって、その信頼性を高めるための試験の実施基準として定められているのが医薬品GLP(医薬品安全性試験実施基準)です。
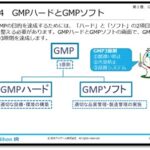
医薬品GLPには、非臨床的な実験研究が計画、実施、監視、記録、報告、保存される組織・体制と過程にかかる原則が定められています。医薬品GLPは、新規医薬品の承認申請資料として用いられる非臨床安全性試験において、その試験の重要性からデータの信頼性をシステムとして保証するためにソフトとハードの両面から規定を定めたものといえます。
その基本構成は、責任体制の明確化、試験方法の標準化、信頼性保証部門の設置、適切な施設設備・機器の使用と管理です。
日本における医薬品GLPは、薬機法(旧薬事法)下の厚生労働省令である「医薬品の安全性に関する非臨床試験の実施の基準に関する省令(平成9 年,厚生省令第21 号)」(医薬品GLP省令)にその基準が定められ、企業や研究機関が守るべき基準として厳密に運用されています。
なお、日本では医薬品GLPの他に、医療機器GLP、再生医療等製品GLP、動物用医薬品GLP、農薬GLP、食品GLP、化学物質(化審法)GLP、労働安全衛生法(安衛法)GLPなどがあります。
2.医薬品GLP省令の概要
医薬品GLP省令は以下の構成となっています。
第一章 総則(第一条―第四条)
第二章 職員及び組織(第五条―第八条)
第三章 試験施設及び機器(第九条・第十条)
第四章 試験施設等における操作(第十一条・第十二条)
第五章 被験物質等の取扱い(第十三条・第十四条)
第六章 試験計画書及び試験の実施(第十五条・第十六条)
第七章 報告及び保存(第十七条・第十八条)
第八章 複数の場所にわたって実施される試験(第十九条)
附則
第1条では、その趣旨が次のように記載されています。
(趣旨)
第一条 この省令は、…厚生労働省令で定める基準のうち、医薬品の安全性に関する非臨床試験…の資料のうち急性毒性、亜急性毒性、慢性毒性、遺伝毒性、催奇形性その他の毒性に関するものの収集及び作成のために、試験施設又は試験場所において試験系を用いて行われるもの…
GLP省令には、次のことが規定されています。
運営管理者は、試験施設の運営管理、計画書等や標準操作手順書(SOP)の作成・記録・保存を行います。また、信頼性保証部門(QAU/Quality Assurance Unit)責任者、資料保存施設管理責任者の指名を行います。
試験責任者は試験計画書を作成し、承認を受けます。また、試験実施が試験計画書および標準操作手順書を遵守しているかを精査します。最終報告書も試験責任者が記録します。
信頼性保証部門(責任者)は、試験関係者以外の者が任命され、試験計画書、試験実施の保証を調査、勧告、再調査します。
試験業務を外部委託する場合は、GLP省令に従って、契約を交わす必要があります。
その他にも、下記のような内容について定められています。
- 設備や機器の使用管理
- 生データ・標本等の整備保存等
- 動物の飼育管理
- 被験物質・対照物質の取扱い
- 試薬および溶液の表示・保管
- コンピュータ調査
- トキシコキネティクス(TK)試験
- 遺伝毒性試験
- 安全性薬理コアバッテリー試験
- 複数場所試験
3.GLP制度の歴史
GLP制度は以下のような経緯で現在に至っています。
- 1972年:ニュージーランドおよびデンマークでGLP制度制定。
- 1976年:バイオテスト工業試験場(Industrial Bio Test Laboratory)が、企業から委託されて行った化粧品、農薬、医薬品など化学物質の安全性試験について、FDAに提出されたデータの多くに捏造が見つかり大問題となった。新薬の承認申請の際に提出された前臨床試験のデータに改竄や捏造、省略などが頻発。
- 1978年:アメリカでGLP制度制定(1979年に発効)。睡眠薬サリドマイドによる薬害事故があり、その非臨床試験の安全性の試験に虚偽や捏造があったことが契機。
- 1981年:経済協力開発機構(OECD)がGLP基準を策定。これを元にしたGLPの導入を各国に求めた。
- 1982年:日本で薬発第313号が公布。薬事法による医薬品等の開発のために行われる非臨床試験(動物試験等、特に安全性試験)のデータの信頼性を確保するための実施基準としてはじめて導入。
- 1983年:医薬品の安全性試験についてのGLP基準が施行。
- 1984年:化審法GLP制度制定。
- 1997年:厚生労働省令第21号「医薬品の安全性に関する非臨床試験の実施の基準に関する省令」(医薬品GLP/ 2008年6月改正・第114号)。食品衛生検査施設にもGLPが導入されることが決定。
- 2005年:厚生労働省令第37号「医療機器の安全性に関する非臨床試験の実施の基準に関する省令」(医療機器GLP/ 2008年6月改正・第115号)。
以上今回は、非臨床試験のルール「GLP制度」の概要について簡単にご紹介しました。
(日本アイアール株式会社 A・A)
<参考資料>
- (1) 「最近のGLP適合性調査について」独立行政法人 医薬品医療機器総合機構(PMDA)
- (2) 「各種関連通知(医薬品・医療機器・再生医療等製品GLP 省令など)(PMDAサイトのページ)
- (3) 「医薬品の安全性に関する非臨床試験の実施の基準に関する省令」(平成9 年,厚生省令第21 号)
- (4) 「GLPとは」 製薬業界 用語辞典 Answers(アンサーズ)
- (5) 「GLPとは何か」日本薬理学雑誌130 巻 (2007) 5 号 p. 403-407
- (6) 「GLP の制定の経緯,必要性及び基礎研究における信頼性に関する課題」薬学雑誌139, 875-879 (2019)
- (7) 「医薬品の研究開発にかかる規制:倫理,ガイドライン,法令の基礎」保健医療科学 2015 Vol.64 No.4 p.382−391