3分でわかる イオン液体とは何か?注目される理由や用途例などを解説

本記事では機能性素材として用途開拓が進行中の「イオン液体」について、その基本事項を解説します。
1.イオン液体とは
イオン液体は、「100℃以下の融点を有する塩であり、イオンのみからなる液体」と定義される化合物群です。
塩と言えばNaCl(融点801℃)に代表されるように無機で高融点のものを想起される方が多いと思いますが、イオン液体の多くは常温で液体です。1990年頃から開発が始まった比較的新しい素材です。
塩ですから、当然ながらカチオンとアニオンとで構成されています。
典型的なイオン液体である1-ブチル-3-メチルイミダゾリウムボロンテトラフルオライドの構造を図1に示します。この化合物の融点はマイナス70℃です。
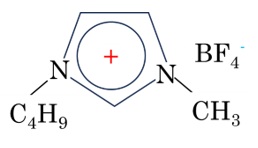
【図1 1-ブチル-3-メチルイミダゾリウムボロンテトラフルオライド】
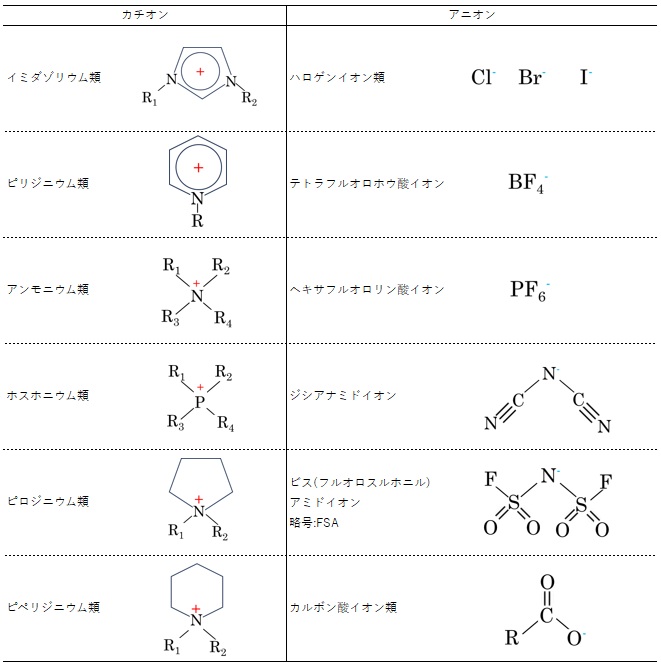
イオン液体を構成可能な代表的なカチオンとアニオンを表1に示します。カチオンとアニオンの組み合わせを選択できますので、多種類のイオン液体が合成可能です。構造設計の自由度が高い化合物群と言えます。
【表1 イオン液体を構成する代表的なカチオンとアニオン】
イオン液体の特徴(メリット・デメリット)
低融点であることを含めて、イオン液体は下記の特徴を有しています。
- 常温常圧下で液体
- 水や空気に対して安定
- 蒸気圧がほぼゼロ
- 難燃性
- 低粘性
- 分解電圧が高い
イオン液体が注目されているのは、これらのメリットをすべて兼ね備えた高機能性素材であるためです。
イオン液体とは“溶媒と無機イオン結晶の両者のメリットを兼ね備えた備えた特異な化合物群”と表現してもよいでしょう。既存の化合物では困難なことがイオン液体で実現できる可能性があります。
一方で、精製に手間がかかるために高価であること、蒸留精製が出来ないために再生利用に難があることがデメリットとして指摘されています。また長期間の使用により未知の毒性副生物が生じる可能性も否定できないので、安全性の検証も課題です。
2.イオン液体はなせ液体なのか?
イオン液体は何故で液体なのでしょうか。塩が常温で液体だということは、換言すれば、塩ではあるものの結晶性が低いということです。
では、結晶性が低いのは何故でしょうか?
塩の分野では、下記の3要素が結晶性を低下させるための主要な要素として知られています。
- 要素(1) カチオンとアニオンの間のクーロン相互作用を弱めること:
両者の距離を広げるために嵩高いイオンを導入するのが有効 - 要素(2) イオン配列の規則性を乱すこと:
非対称構造のイオンの導入が有効 - 要素(3) 柔軟な構造を導入すること:
ある程度の長さのアルキル鎖の導入が有効
この3要素がイオン液体の合成に積極的に導入されています。
その効果の大きさを具体的に検証してみましょう。
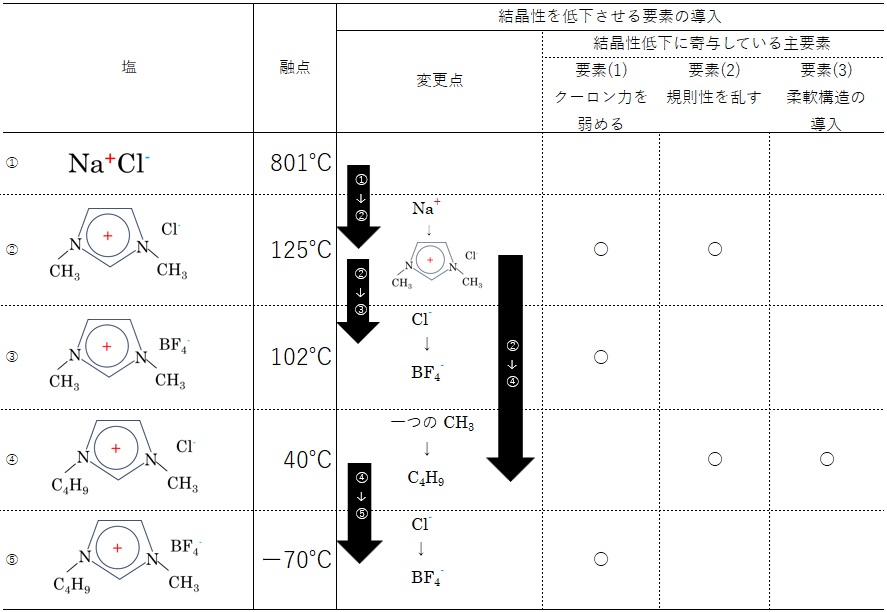
表2はNa+Cl–を出発材料にして、イミダゾリウム系カチオンを有するイオン液体を対象に、結晶性を低下させる要素導入の効果を検証したものです1)。
表2で塩①Na+Cl–のNa+を1,3-ジメチルイミダゾリウムに変更して塩②にすると、融点が801℃から125℃に低下しています。これはイオン間の距離が広がってクーロン力を弱める要素(1)と、規則性を乱す要素(2)が寄与していると考えられます。
融点−70℃の塩⑤1-ブチル-3-メチルイミダゾリウムボロンテトラフルオライドに至る過程における上記3要素の効果の大きさが、表2から確認できます。
【表2 結晶性を低下させる要素をイオン液体に導入した効果】
3.イオン液体の合成
イオン液体はアニオン交換法または中和法によって合成することが出来ます。
イミダゾリウム系カチオンを有するイオン液体の例を図2に示します。
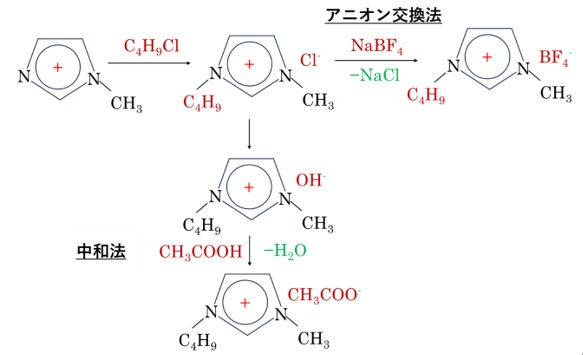
【図2 イオン液体の合成例】
4.イオン液体の用途
イオン液体は、揮発性の低さと特異な溶解性を活かした有機合成用溶媒、イオン導電性を活かした電解質、更には合成用触媒等として、多くの分野で用途開拓が進行中です。詳細は成書でご確認下さい2),3)。
[※関連記事:リチウムイオン電池の電解液② スルホンアミド系、イオン液体、水系 ]
本コラムでは、他素材では実現困難な特性が発揮されている下記2例を紹介します。
(1)セルロース溶解能
セルロースは草本系バイオマスの主要構成分であり、また資源量も豊富ですので、その有効活用が期待されています。しかし、セルロースを溶解できる溶媒がほとんど無いために、利用があまり進んでいません。
その中で、1-ブチル-3-メチルイミダゾリウムクロライド等の特定のイオン液体がセルロース溶解能を有することが2002年に報告されて以降、イオン液体が注目を集めています。イオン液体が高価なため、このセルロース溶解能の工業的な利用はまだ進んでいませんが、木材用接着剤に応用できる可能性が報告されています。
[※関連記事:イオン液体のセルロース溶解能をどう活用する?注目の研究開発動向を紹介 ]
(2)電子顕微鏡観察への利用
電子顕微鏡は、高真空中に試料を置いて電子線照射により微細構造を観察する非常に有用な分析機器です。現代の科学の進展を支えています。
しかし、生体試料等の絶縁体を観察する際には、試料表面に金等を予め蒸着する必要があります。この蒸着では、試料がダメージを受けてしまい、本来の状態の観察が困難になることがしばしばあります。
これに対して、イオン液体は導電性を有する液体であり高真空中でも揮発しないため、試料にイオン液体を含浸させれば、試料本来の姿を観察することが出来ます。生体試料の細部を金蒸着よりも高精度で観察した例が報告されています4)。
5.イオン液体の類似材料:深共晶溶媒
イオン液体と類似の材料で近年注目されている材料に深共晶溶媒(Deep Eutectic Solvent)があります5)。
深共晶溶媒は、「a)水素結合ドナー性の化合物とb)水素結合アクセプター性の化合物(両方か又はどちらか一方が固体)をある一定の割合で混合して生成する、室温で液体になる混合溶媒」と定義されています。 a)とb)が室温で固体であっても、混合により共晶融点降下が起こり、室温で液体状態になります。
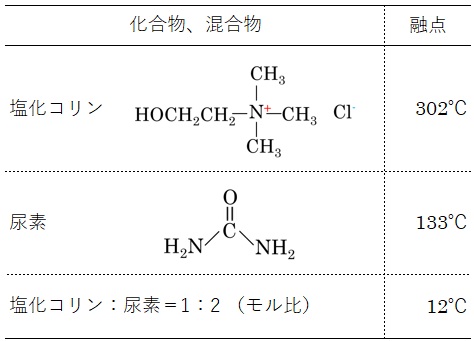
代表的な深共晶溶媒として、塩化コリン:尿素=1:2 (モル比)の混合物が挙げられます。
表3をご覧ください。この混合物の融点は、混合原料のどちらの融点よりもはるかに低い12℃となっています。
深共晶溶媒は不揮発性や不燃性ではイオン液体に劣るものの、2成分を混合するだけで生成するのでイオン液体に比べて低コストです。また、イオン液体に比べて環境親和性が高く、有毒なものが少ないという特徴もありますので、イオン液体の弱点を補える可能性があります。
このため、イオン液体が検討されている分野への適用が進行中です。
[※関連記事:推進剤としてのイオン液体と深共晶溶媒 ]
【表3 代表的な深共晶溶媒】
以上、今回はイオン液体の基本事項について解説しました。
上述のようにイオン液体は、その特異な物性と応用範囲の広さから、今後の材料開発やプロセス革新において重要な役割を果たすことが期待されます。応用例も年々多様化しており、基礎研究と産業応用の両面で活発な取り組みが進んでいます。今後もその技術動向に注目し、柔軟な視点での応用展開を探っていくことが求められます。
(日本アイアール株式会社 特許調査部 N・A)
《引用文献、参考文献》
- 1) 下記データ等に基づいて作成
Suojiang Zhang etc., Physical Properties of Ionic Liquids: Database and Evaluation, J. Phys. Chem. Ref. Data 35, 1475–1517 (2006) - 2) 西川恵子他, イオン液体, 共立出版(2021)
- 3) 高分子学会編, イオン液体, 共立出版(2012)
- 4) 桑畑進, イオン液体の液状導電付与剤としての電子顕微鏡観察への応用, 顕微鏡48(2), 100-106(2013)
https://www.jstage.jst.go.jp/article/kenbikyo/48/2/48_100/_article/-char/ja/ - 5) Emma L. Smith etc., Deep Eutectic Solvents (DESs) and Their Applications, Chem. Rev., 114(21), 11060–11082(2014)
https://pubs.acs.org/doi/epdf/10.1021/cr300162p?ref=article_openPDF