エンドトキシン試験の実務知識を初心者向けに解説 (試験法/管理/バリデーション等)

医薬品や医療機器の製造において、「エンドトキシン」(内毒素)の管理は、品質保証の中核をなす要素の一つです。特に注射剤やインプラント製品といった、体内に直接使用される製品では、エンドトキシン汚染が人体に深刻な影響を与える可能性があるため、厳格な試験と管理が求められます。
この記事では、エンドトキシン試験の基礎から、エンドトキシン管理における実務的なポイント、規格値の設定、バリデーション、そしてデータインテグリティやコンピュータ化システムバリデーション(CSV)に関連する最新の考え方までを総合的に解説します。
目次
1.エンドトキシンとは?
「エンドトキシン」は、グラム陰性菌の外膜を構成するリポ多糖(LPS)成分であり、菌が死滅・分解された際に放出されます。発熱や炎症、さらにはショック症状などを引き起こす原因となるため、特に注射剤などの無菌製品においては、極微量でも存在してはならないとされています。
(※エンドトキシンの基礎知識は、別記事「3分でわかる エンドトキシンとは?」もご参照ください)
2.エンドトキシン試験の方法
エンドトキシン試験は、医薬品や医療機器などの製品にエンドトキシン(内毒素)が混入していないかを確認するために実施される、非常に重要な品質試験です。
日本薬局方(JP)、米国薬局方(USP)、欧州薬局方(EP)では、基本的にリムルス試験(LAL試験:Limulus Amebocyte Lysate Assay)が規定されており、3つの主要な測定法が使用されます。
エンドトキシン試験の基本原理のイメージは図1をご参照ください。
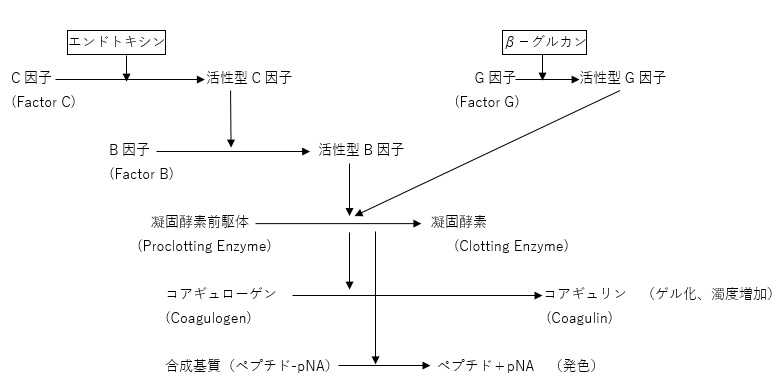
【図1 リムルス試験の基本原理】
(※「3分でわかる エンドトキシンとは?」の図1を再掲)
以下、3つの測定法の原理と特徴、使用上の注意点について詳しく説明します。
① ゲル化法
「ゲル化法」(Gel-Clot法)は、LAL試薬がエンドトキシンと反応することでゲル(ゼリー状)を形成する現象を利用した半定量試験です。一定時間(通常60分)後に試験管を傾けて、ゲルが崩れなければ陽性と判断されます。
この方法の特徴としては、機器を必要とせず、目視による判定が基本となるため、操作がシンプルという点が挙げられます。また、試験試料がエンドトキシン反応に及ぼす影響、すなわちインターフェア(阻害や増強)を比較的容易に検出できるという利点もあります。
一方で注意すべき点として、判定が人の目に依存するため、主観的な要素が含まれることがあります。また、反応の感度は使用するLAL試薬によってあらかじめ規定されており(例えば0.125 EU/mLなど)、その特定の濃度以下での検出は困難であるという制限があります。
② 比濁法
LAL試薬とエンドトキシンが反応すると、凝集により混濁が発生します。「比濁法」(Turbidimetric法)は、この濁度の変化を光学的に測定することで、エンドトキシン濃度を定量します。エンドトキシン濃度が高いほど、混濁が早く進行します。
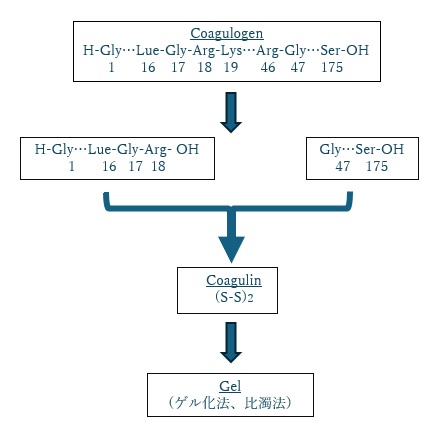
【図2 比濁法の原理】
比濁法の特徴としては、標準曲線と比較することでエンドトキシンの量を正確に定量できることが挙げられます。さらに、マイクロプレートリーダーなどの機器を使用すれば多くの試料を同時に測定できるため、高スループットな運用が可能です。
ただし注意点として、試薬のロット差や測定条件によって感度が変動することがあるため、都度バリデーションを行う必要があります。また、光学的な測定を行うため、試料中の色や濁りが測定に干渉する可能性があることにも配慮が求められます。
③ 比色法
「比色法」(Chromogenic法)は、LAL反応系に発色合成基質を組み込むことで、エンドトキシンが存在すると黄色の発色が生じ、その色の強さを測定することで濃度を定量します。基質の分解はエンドトキシン濃度に比例するため、より高感度な測定が可能です。
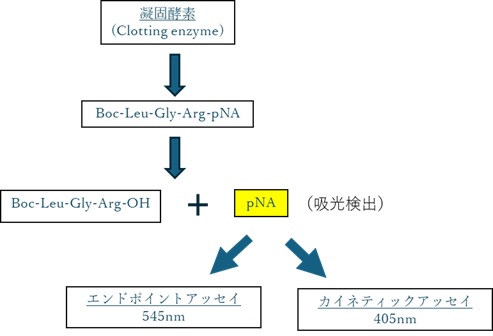
【図3 比色法の原理】
比色法の特筆すべき特徴は、非常に高い感度を持ち、0.005 EU/mL以下まで検出可能なキットも存在する点です。また、自動化機器との親和性が高く、CSV(Computerized System Validation)対応も比較的容易であるため、製薬業界などの品質管理に適した手法と言えます。
一方で注意点としては、発色基質の安定性が測定精度に影響を与える可能性があることや、試料中に比色干渉物質が含まれている場合には誤差が生じやすいことが挙げられます。また、検出限界が非常に低いため、バックグラウンドの管理を厳密に行う必要があります。
3つの方法のどれを用いるのか?
ゲル化法、比濁法、比色法の特徴・用途を整理すると次の表のようになります。
| 試験法 | 主な用途 | 特徴 | 欠点 |
| ゲル化法 | ルーチンのスクリーニング、インヒビション試験 | 安価・簡便 | 主観的、感度に限界 |
| 比濁法 | 定量が必要な製品 | 自動化・高スループット | 試料干渉に弱い |
| 発色法 | 微量検出、高感度要件 | 高感度・自動化適合 | 高コスト、干渉リスク |
なお近年では、比濁法や発色法の自動測定装置が多く使用されるようになっており、測定条件、データ記録、結果出力のトレーサビリティが重視されます。これに伴い、コンピュータ化システムバリデーション(CSV)の対応も不可欠となっています。
[※関連記事:改正GMP省令の重要ポイントを解説!データインテグリティなどの概要がわかる ]
以下の点を満たさない場合、当局監査で指摘される可能性があるため、試験方法選定の段階からCSV要件を念頭に置く必要があります。
- 装置のユーザー要件仕様(URS)の作成
- IQ(設置時適格性確認)、OQ(運転時適格性確認)、PQ(性能適格性確認)の実施
- ソフトウェアのアクセス制御・監査証跡の確認
- 21 CFR Part 11やAnnex 11に準拠した電子記録・電子署名の要件対応
その他の方法(遺伝子組換え因子の使用)
上記3つの方法以外にも遺伝子組換え因子を使用する方法があり、2種類の遺伝子組換えLAL試薬が実用化されています。
カスケード反応に関わる3因子のうち、C因子の遺伝子組換えタンパク質(rFC)だけをを使用した1因子系試薬と、3因子(C因子、B因子、凝固酵素前駆体)の遺伝子組換えタンパク質recombinant cascade reagent(rCR)を使用した3因子系試薬の2種類に分類されます。
1因子系試薬であるrFCのみを使用する試薬は、3因子系試薬に比べ、1テスト当たりの費用は抑えられます。しかし、カスケード反応による増幅がないため、生成するプロテアーゼ活性が小さく蛍光基質を使用した蛍光検出を行う必要があります。
一方、3因子系試薬は、1因子系試薬に比べて感度が高く、発色基質を使用できるため従来型のLAL試薬による比色法と同様一般的なプレートリーダーで測定可能です。
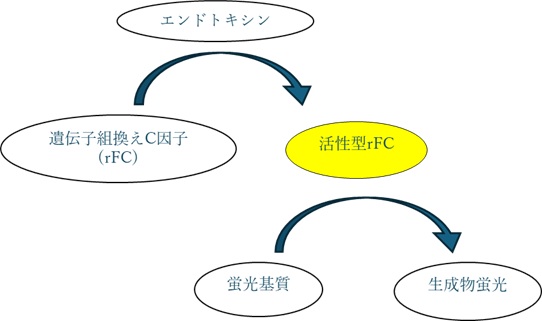
【図4 遺伝子組換えC因子】
3.エンドトキシンの規格値設定と法的基準
エンドトキシンの規格値は、製品の最大投与量や投与ルートに基づき、1時間あたりの許容エンドトキシン量(Endotoxin Limit)として定義されます。
例えば、静脈注射剤の一般的な規格値は「5 EU/kg/時」とされており、体重60kgの患者に対して1時間あたり300EUが上限となります。製品ごとにこの基準値をもとに規格値を設定し、ロットごとの試験結果がこの値以下である必要があります。
4.エンドトキシン試験とバリデーション
エンドトキシン試験を実施する上では、試験法が対象製品に適合しているかどうかを評価するためのバリデーション(妥当性確認)が求められます。具体的には、以下のような確認・検証を行う必要があります。
- 回収率試験(インヒビション/エンハンスメント試験):
試料中に存在する成分が試験結果に影響しないかを検証します。 - 感度の確認:
試薬の感度が規格に適合しているかを確認します。
また、設備や工程そのもののバリデーション(例:高温滅菌バリデーション)もエンドトキシン管理には不可欠です。
5.データインテグリティとCSVの重要性
近年、GMP運用において最も注目されているのが、データインテグリティ(Data Integrity)とコンピュータ化システムバリデーション(CSV)です。
エンドトキシン試験も例外ではなく、試験データの信頼性を確保するために以下のポイントが重視されます。
- ALCOA原則(Attributable, Legible, Contemporaneous, Original, Accurate:データの真正性と一貫性を保証するための原則)
- 電子記録・電子署名の適切な運用(21 CFR Part 11)
- 試験機器(比濁計、発光計など)のCSV実施
たとえば、発光法を用いた自動測定システムでは、試験条件、試験ログ、測定データの保存と追跡性が担保されていることが不可欠です。CSVを通じて、コンピュータシステムの信頼性を高め、監査時にも耐えうる体制を整えることが求められます。
6.まとめ:エンドトキシン管理の今とこれから
エンドトキシン試験は、単なる試験操作ではなく、製品品質と患者安全性を保証するための総合的な管理活動です。エンドトキシン汚染の防止、規格値の適切な設定、妥当性確認、さらにCSVやデータインテグリティの対応まで、広範な知識と技術が求められます。
GMP遵守がますます強化される中で、エンドトキシン管理に携わる技術者や品質保証担当者には、実務知識の継続的なアップデートが不可欠です。
エンドトキシン試験に関する最新の規制動向や、バリデーション、CSV対応の実務に即した知見を深めたい方には、セミナーの受講をお勧めします。実際のトラブル事例や当局査察の傾向など、現場で役立つ内容を専門家が詳しく解説します。
(日本アイアール株式会社 特許調査部 A・A)
《引用文献、参考文献》
- 富士フイルム和光純薬株式会社(WEBサイト)
【Wako LALシステム】「エンドトキシン測定について」
https://labchem-wako.fujifilm.com/jp/lal/lal_knowledge/about_lal02.html
【テクニカルレポート】遺伝子組換えタンパク質を用いたエンドトキシン測定試薬
https://labchem-wako.fujifilm.com/jp/siyaku-blog/035291.html
https://labchem-wako.fujifilm.com/jp/siyaku-blog/040437.html - 蓜島 由二「エンドトキシン試験における留意点」
https://www.nihs.go.jp/kanren/iyaku/20190521-dmd-1.pdf - ロンザ株式会社 PyroGene® Recombinant Factor C エンドトキシン検出システム(カタログ)
https://www.lonzabio.jp/catalog/pdf/ri/I613.pdf - PyroSmart NextGen® 遺伝子組換えLAL試薬(取扱説明書)
https://www.acciusa.com/pdfs/accProduct/PyroSmart_multilang_IFUs/PyroSmart_NextGen_IFU_PN002641r4_JA.pdf
- エンドトキシン試験法の基礎と実践(講師:田村弘志 氏)