セルバンクの種類とセルバンク化プロセスをやさしく解説《バイオ医薬品製造の基盤》
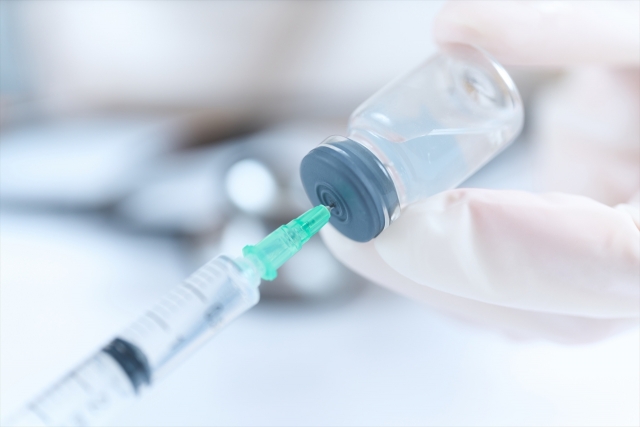
バイオ医薬品とは、遺伝子組換え技術や細胞培養技術を駆使して製造される医薬品で、抗体医薬品やタンパク質医薬品などが含まれます。これらの製品の品質、安全性、一貫性、再現性を確保するためには、製造の起点となる「細胞」の管理が極めて重要です。その中核的な役割を果たすのが「セルバンク」(Cell Bank)です。
目次
1.セルバンク化とは何か?
「セルバンク」とは、製造に使用する細胞株を凍結保存し、品質が保証された状態で保管する仕組みのことです。バイオ医薬品では、同一の細胞株を用いて一貫して製造する必要があるため、製造初期段階で信頼性の高い「種」となる細胞をストックしておくことが不可欠です。
セルバンク化はなぜ重要なのか?
セルバンク化が求められる理由として、主に以下の点が挙げられます。
- 製造の一貫性確保:
同一のセルバンク由来の細胞を使用することで、製品間のばらつきが抑えられます、 - 品質管理・トレーサビリティ:
問題が発生した場合でも、セルバンク由来まで遡って原因究明・是正が可能です。 - 規制対応(GMP):
医薬品の製造にはGMP(Good Manufacturing Practice)準拠が義務付けられており、バイオ医薬品の場合、GMP準拠施設でのセルバンクの製造・保管が必須であり、セルバンクの分散保管施設もGMP準拠施設であることが必要です。
[※関連記事:《医薬品製造関係者の常識》GMPって何?|GMPの3原則など必須前提知識をチェック!]
2.セルバンクの種類
バイオ医薬品のセルバンクには、開発段階で抗体などの目的物質を多く産生する細胞を作製する必要があり、「リサーチセルバンク」(Research Cell Bank:RCB)と呼ばれます。
バイオ医薬品の製造段階では、「マスタセルバンク」(Master Cell Bank:MCB)と「ワーキングセルバンク」(Working Cell Bank:WCB)という2段階の構造があります。これは、製品の一貫性と品質を保証するために極めて重要です。
(1)リサーチセルバンク(RCB)
リサーチセルバンク(RCB)は、宿主細胞(抗体医薬品であれば、主にCHO細胞)に目的タンパク質の遺伝子をプラスミドに組み込み、発現ベクターを作製し、宿主細胞へ発現ベクターを導入することで目的タンパク質の産生細胞株を作製します。
組換え細胞は細胞間でタンパク質の産生に差があるため、製造に適した細胞をスクリーニングします。
(2)マスタセルバンク(MCB)
マスタセルバンク(MCB)は、製造に使用する細胞株を高純度・高品質な状態で凍結保存した「種」にあたるものであり、製造プロセスにおける全ての細胞の起点となります。
クローン細胞であるRCBは一般的に10本程度のバイアルに分注されており、そのうちの1本を培養して数百本単位のバイオあるに分注され、MCBは作製されます。
マスタセルバンクの主な特徴
- 単一細胞由来のクローンである(遺伝的均一性の確保)
- 通常、数百~数千バイアルが液体窒素で保存される
- 品質管理試験(QC)が厳格に実施される(表1:セルバンクの品質項目例)
【表1 セルバンクの品質項目例】
| 試験項目 | 目的 |
| 無菌性試験 | 細菌や真菌の汚染有無の確認 |
| ウイルス否定試験 | 細胞がウイルスに汚染されていないか確認 |
| マイコプラズマ否定試験 | マイコプラズマの検出 |
| アイソザイム解析 | 細胞の同一性の確認。異種細胞の混入を検出 |
| 遺伝子安定性確認 | 長期保存後でも変異がないかを評価。シークエンス解析による塩基配列確認試験、サザンブロッティングによるコピー数の確認試験等 |
| 形態観察試験 | 参照写真との比較 |
| 増殖試験 | 細胞の倍加時間や増殖速度の評価 |
マスタセルバンクの保存と取り扱い
保存温度は−135℃以下(液体窒素中、または超低温冷凍庫)です。
マスタセルバンクは製造時に直接使用することはなく、ワーキングセルバンクの構築時にのみ使用します。
(3)ワーキングセルバンク(WCB)
WCBは、MCBの1本のバイアルより培養し、新たに凍結保存した細胞群です。
実際の製造ロットでは、このWCBから培養された細胞が使用されます。
ワーキングセルバンクの主な特徴
- MCBから派生しているため、由来が明確
- 製造ごとに直接使用されることで、MCBを頻繁に解凍せずに済む
- WCB自体も一定の品質試験を受けるが、MCBほどの厳密性は不要
ワーキングセルバンクの利用サイクル
- MCBから数十バイアルのWCBを作成
- 各製造ロットにおいて、WCBから細胞を解凍・培養
- 製品を製造
- 必要に応じて再度WCBを作成(ただしWCBはMCBから直接派生したもののみとする)
3.セルバンク化のプロセス
セルバンク化は、一般的に以下のような工程で行います。
- 細胞株の選定:
高収量・安定性・目的タンパク質の生産能力を基準に細胞株が選ばれます。CHO細胞が代表的です。 - クローニング・単一化:
単一の細胞から増殖させることで、遺伝的に均一な細胞株を確立します。 - マスタセルバンクの構築:
大量培養した細胞を凍結保存。凍結保存には液体窒素(−196℃)が用いられます。 - 品質評価試験:
無菌性、ウイルス不在、細胞同定、形態安定性など、多数の試験項目を実施して品質保証をします。 - ワーキングセルバンクの構築:
MCBの一部を培養してWCBを構築。これも凍結保存されます。
図1に抗体医薬品開発における、遺伝子組換えによるRCBの構築、MCB/WCBの作製、その後の抗体医薬品の製造までの簡単なプロセスを示します。
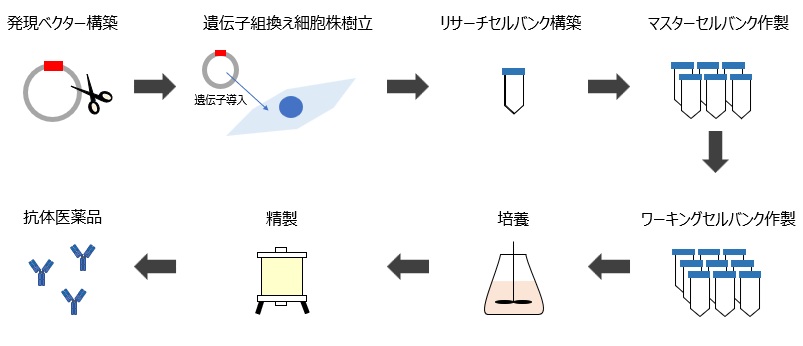
【図1 セルバンク化の流れ】
4.セルバンク化に関する課題
現在では、遺伝子導入技術や自動化装置によりセルバンク構築の効率も高まりつつあります。一方で、以下のような課題も指摘されています。
- 長期保存における細胞劣化の懸念
- 試験法や承認要件の国際的整合性の確保
- 細胞治療・再生医療製品における「患者由来セルバンク」の管理問題
セルバンク化は、バイオ医薬品の製造における品質の起点であり、安全性・再現性・規制対応のために不可欠な基盤技術です。バイオ医薬品の発展や技術革新に伴い、今後より高度なセルバンク管理が求められるため、細胞株構築とセルバンク化の基本をしっかりと押さえておくことが重要となります。
(日本アイアール株式会社 特許調査部 N・Y)
- バイオ医薬品生産用の遺伝子組換え体細胞の構築とセルバンク化(講師:片山政彦 氏)