核酸ワクチンが基礎からわかる!従来型とは何か違うのか?種類,仕組み,特徴を解説

新型コロナウイルス感染症(COVID-19)の対策としてワクチン開発が重要となっています。
現在、mRNAワクチンをはじめとする核酸ワクチンが注目され、国内でも開発が急ピッチで進んでいます。今回は従来型ワクチンと次世代型の核酸ワクチンについて基礎から解説していきます。
1.従来型ワクチン
従来型のワクチンは感染症の病原体を弱毒化・無毒化してヒトの体内に投与することで、病原体に対する抗体を産生させ免疫を獲得することにより、感染症にかかりにくく重症化を防ぐ目的として製造されています。
従来型のワクチンとしては以下のようなタンパク質型ワクチンが主として用いられてきました。
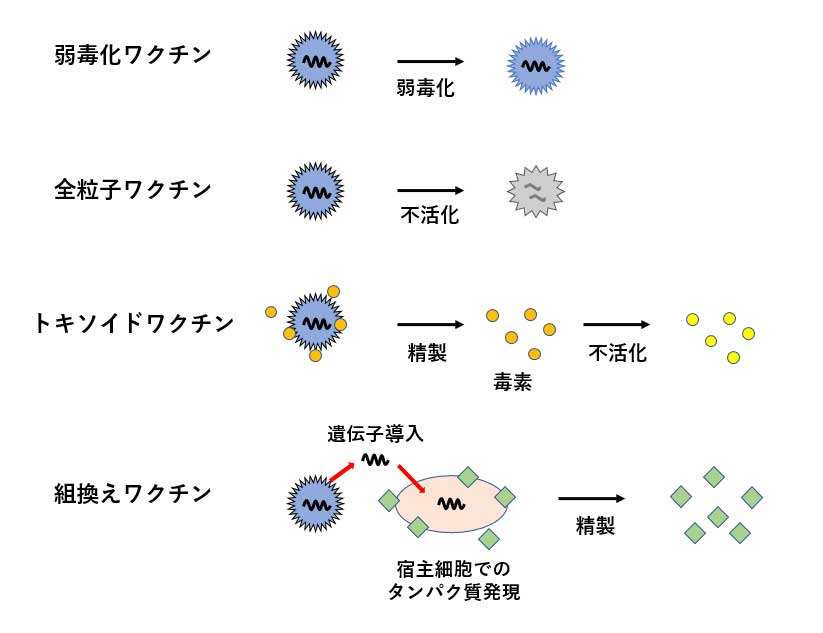
[図1:従来型ワクチンの製造法]
(1)生ワクチン(弱毒化ワクチン)
症状がでない程度まで弱毒化したウイルスや細菌を製剤として投与し、弱毒化された病原体が体内で増殖するため、自然免疫に近い形で免疫が得られ免疫獲得への効果が強い一方、副反応の可能性も高く、また弱毒化株の樹立には長い時間を要します。
(2)不活化ワクチン
① 全粒子ワクチン
全粒子ワクチンは、ウイルスや細菌などの病原体を加熱や紫外線、化学処理することにより、感染性や病原性をなくした病原体を用います。
② サブユニットワクチン
サブユニットワクチンは、免疫獲得に必要となる成分を抗原として抽出して用います。
③ トキソイドワクチン
トキソイドワクチンは、病原体から産生される細菌毒素を取り出し、薬品処理し不活化・精製することで無毒化した毒素を抗原として用います。
④ 組換えワクチン
組換えワクチンは、ウイルスの抗原となる部分の遺伝子を宿主細胞へ導入して、細胞に産生させた組換えタンパク質を用います。必要な抗原だけ発現させた組換えタンパク質によるサブユニットワクチンやカプシドと呼ばれるウイルスの表面タンパク質のみでウィルスゲノムを持たないウイルス様粒子(VLP)などがあります。
2.次世代型核酸ワクチン
一方、COVID-19ワクチンでも注目されている核酸ワクチンは従来のタンパク質型ワクチンとは異なり、抗原タンパク質を体内へ投与するのでなく、抗原タンパク質をコードする遺伝子を投与し、体内で抗原となるタンパク質を産生させるワクチンです。
不活化ワクチンと比較すると抗体を産生する液性免疫だけでなく細胞性免疫の効果が期待できます。図2のように体内で病原体由来の抗原が抗原提示細胞に取り込まれ、抗原の一部をTヘルパー細胞へ提示し、ヘルパーT細胞によりB細胞が活性化し、抗体産生細胞として抗体の産生を行うことや、細胞障害性T細胞による細胞性免疫を誘導します。
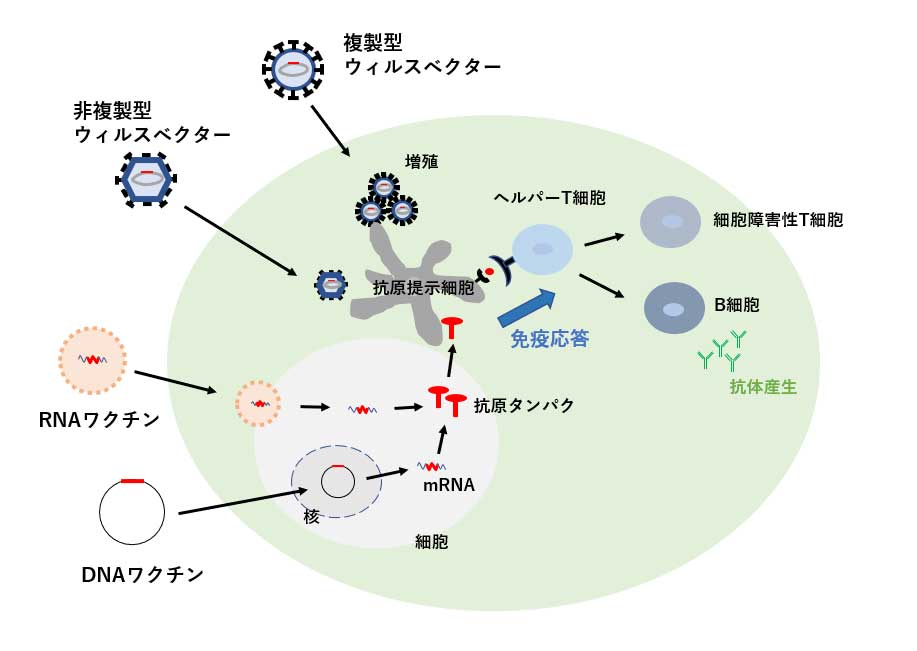
[図2:次世代型ワクチンの作用機序]
(1)ウイルスベクターワクチン
ウイルスベクターワクチンは病原体とは別の病原性のないウイルスベクターに抗原タンパク質をコードする遺伝子を組み込んだ組換えウイルスを体内へ投与することで、細胞内で抗原タンパク質を産生させ、免疫が誘導されます。
体内で複製し増殖する複製型ウイルスベクターと、増殖に関する遺伝子が失われ増殖できない非複製型ウイルスベクターがありますが、実用化されているアストラゼネカ社のCOVID-19ウイルスベクターワクチンはチンパンジーアデノウイルスを用いたもので非複製型になり、ベクターに感染の足掛かりとなるスパイクタンパク質の遺伝子を組み込まれており、スパイクタンパク質に対する免疫が誘導されます。
ウイルスベクターワクチン自体は、COVID-19以前にすでにエボラ出血熱のワクチンとして実用化されており、また冷蔵保管できる点もメリットがあります。
(2)RNAワクチン
mRNAは細胞内でDNAから遺伝情報を転写して作られ、この情報をもとにタンパク質が合成されます。この機構を利用し、mRNAワクチンは抗原をコードする人工的に作成したmRNAを投与し、抗原タンパク質を体内で合成させます。
mRNAは体内で分解しやすい不安定な分子のため、脂質ナノ粒子などのキャリア分子にmRNAをカプセル化され、細胞膜とキャリア分子の脂質膜が融合されることでmRNAが細胞質に送達されます。
分解しやすいという点については、RNA分子の修飾方法やキャリア分子の改良によって改善されてきていますが、製剤として超冷凍保管が必要など課題もあります。mRNAワクチンは核内への移行が不要のためゲノム挿入のリスクがなく、また他の方法と比べて短期間に容易に設計が可能な点がメリットになります。
COVID-19ワクチンとしてはファイザー社がmRNAワクチンとして初めて実用化され、国内では第一三共社が臨床試験へ進む見込みです。
(3)DNAワクチン
DNAワクチンは抗原タンパク質をコードする遺伝子を組み込んだプラスミドDNA(環状DNA)ワクチンで、プラスミドそのものを投与し、核内でmRNAに転写され細胞質で抗原タンパク質を産生させるため、mRNAワクチンと比べて転写と翻訳の2ステップの工程が必要となります。
免疫原性(抗体の産生や細胞性免疫を誘導する性質)が低いという課題については、接種後にエレクトロポレーション(電気刺激)により細胞膜の透過性を高めてDNAの細胞膜への取り込みを高める方法や免疫効果を増強するアジュバンドを添加する方法を用いています。
また生産に関しては、プラスミドDNAを大腸菌に導入することで短期間に大量生産することが可能で、保管についても通常の冷凍温度で保管が可能です。COVID-19ワクチンとしてはイノビオ社や国内ではアンジェス社がDNAワクチンの開発を進めています。
COVID-19の拡大により核酸ワクチンが注目されていますが、核酸医薬品としてはすでに癌治療や遺伝子疾患治療、再生医療の分野でも研究が進んでいるため、今後核酸医薬品の開発や実用化が期待されます。
(日本アイアール株式会社 特許調査部 N・Y)