《速習解説》ペプチド医薬品の概要 [前提知識/特徴と課題/製造方法/開発動向など]

未だに有効な治療方法がない疾患おいて、未だ満たされていない医療ニーズは「アンメット・メディカル・ニーズ」と呼ばれています。ペプチド医薬品は、今後アンメット・メディカル・ニーズを満たしてくれる医薬品として期待されています。
ではなぜ、ペプチド医薬品が期待されているのでしょうか?
近年注目されているペプチド医薬品について解説します。
目次
1.ペプチドとは?
トリプトファン、フェニルアラニン、ロイシン、アスパラギン、グルタミン酸などのわずか20種類のアミノ酸が、私たちのカラダを構成する10万種類にも及ぶタンパク質を作っています。ヒトのカラダの約20%がタンパク質でできていますので、アミノ酸は私たちの生命にとってとても重要な物質です。
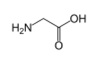
【図1 グリシン(最もシンプルなアミノ酸)】
「アミノ酸」とは、アミノ基とカルボキシ基の2つの官能基を持つ有機低分子の総称です。
このアミノ酸同士がアミノ基とカルボキシ基の脱水縮合によってアミド結合を形成することで作られる物質が「ペプチド」です。このペプチドが幾つもアミド結合で繋がって、高分子のタンパク質を作っていきます。
ペプチドとタンパク質の呼称については、その分子量などで明確に定義されていませんが、おおよそアミノ酸数が50前後で区別されています。
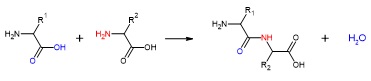
【図2 アミノ酸の脱水縮合によるアミド結合形成】
2.生理活性と課題
(1)生理活性を持つペプチド
生体において、ペプチドは神経伝達物質、局所ホルモンなどの役割を担っており、神経系、平滑筋、心臓血管系、免疫系など様々な機能に関与しています。この様なペプチドは「生理活性ペプチド」と呼ばれ、血液中での酵素反応による生成、あるいは神経やその他諸組織に内在しています。
生理活性ペプチドには、β-エンドルフィン、サブスタンスP、バソプレシンなどのニューロペプチドや、エンドセリン、アンギオテンシン、ナトリウム利尿ペプチドといった循環ペプチドなどが知られています。
(2)医薬品としての難しさ(課題)
前述のように生体において様々な生理活性を持つペプチドですが、それらがそのまま医薬品として有効であることは稀です。
例えば、ニューロペプチドのエンケファリンは、鎮痛に係わるオピオイド受容体に作用しますが、現在でも、非ペプチドアナログであるモルヒネが使用されていて、エンケファリン自体またはその類縁ペプチドが用いられることはありません。
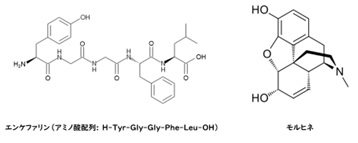
【図3 エンケファリン(Leu-Enkephalin)とモルヒネの化学構造】
一般的に医薬品は、カラダへの負担が少ない飲み薬として経口投与できることが望まれます。
経口投与された医薬品は、主に消化管で吸収されて門脈を経由して肝臓に運ばれ、初回通過代謝を受けたのち全身循環系に入っていきます。
生理活性ペプチドはこのシステムに適応していません。
これは、ペプチドが消化管で吸収される前に、加水分解酵素で速やかに分解されるからです。
また、極性官能基を持つため細胞膜の透過性が低く、医薬品に求められる薬物動態のクライテリアを満たさないため、創薬の対象として、有機低分子などと比べて探索の優先度が低い存在でした。
3.ペプチド医薬品の歴史
(1)ヒトインスリンの登場
1型糖尿病は、膵臓β細胞の破壊により、膵臓ホルモン「インスリン」が欠乏することで発症する疾患です。
この不足したインスリンを補う対処療法として開発されたのが「ヒトインスリン」で、1982年に世界で初めて上市されたバイオ医薬品であり、同時にペプチド医薬品でもあります。日本では1985年に製造承認されています。
インスリンの化学構造は、アミノ酸21個のペプチド(A鎖)とアミノ酸30個のペプチド(B鎖)がS-S結合で連結したポリペプチド(分子量5807.57)です。
インスリンは経口投与ができないため、腹部などに皮下注射により投与されます。
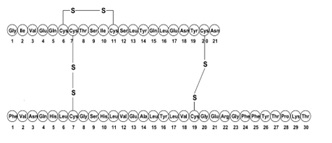
【図4 ヒトインスリンの化学構造】
(2)環状ペプチド医薬品
ペプチド医薬品の代表的な存在が、黎明期(1970年頃)に創出された「シクロスポリン」です。
シクロスポリンは、土壌真菌の代謝産物から分離された中性・疎水性の環状ペプチドで11個のアミノ酸からなる免疫抑制薬です。シクロスポリンは、T細胞機能を介して拒絶反応を強力に抑制する作用を有しており、臓器移植に多大に貢献しています。
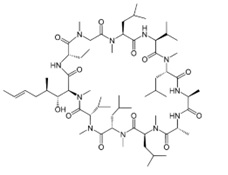
【図5 シクロスポリンの化学構造】
その構造的な特徴はD-アミノ酸を1つ有するペプチドで、イオン性官能基を持たない、多数のアルキル鎖で置換された環状型化合物であることが挙げられます。この構造によって加水分解酵素に対して耐性を獲得し、中性・疎水性といった物性が膜透過性や体内動態などの医薬品に適した性質を付与しています。
シクロスポリンは、経口製剤として開発されている環状ペプチド医薬品です。日本では1985年に注射剤が、2000年に経口剤が承認されています。
4.ペプチド医薬品の製造方法
(1)化学合成
ペプチドの化学的な合成方法は、アミノ酸の反応点となるアミノ基とカルボキシ基以外の官能基を保護基で保護したのち、縮合剤を使ってアミド結合を形成します。
続いて、次の反応点となるアミノ基またはカルボキシ基の脱保護を行い、保護基が導入されたアミノ酸と脱水縮合することで新たにアミド結合を形成させます。
このように保護、縮合、脱保護を繰り返すことで、ペプチドを構築していきます。
このため、ペプチドの製造には膨大な手間とコストが掛かります。
このことが、ペプチド医薬品の探索、開発を妨げていた要因の1つでもあります。
(2)生物学的生産
前述のインスリン製剤は、当初、ブタやウシの膵臓から抽出したインスリンを使用した動物インスリン製剤でした。
但し、ヒトインスリンと動物インスリンの化学構造は同一ではありません。ウシとは3個のアミノ酸が異なりますし、ブタでも1個のアミノ酸が違っています。
その後、ヒトインスリンに構造が近いブタインスリンから、ペプチド転移反応により直接ヒトインスリンを半合成する手法が開発され、1982年にヒトインスリンが発売されることになります。現在では、遺伝子組み換え大腸菌の大量培養によってヒトインスリン製剤は生産されています。
シクロスポリンも同様で、真菌の変異株の培養液から分離する生物学的な生産方法となっています。
5.なぜ、ペプチド医薬品か?
シクロスポリンが示しているように、環状ペプチド(中分子)の医薬品としてのポテンシャルは高いに違いありません。
抗体などの高分子バイオ医薬品と比べて、経口吸収性や膜透過性は優れていますし、適当な自由度を持った環状ペプチド構造は、生体のタンパク質とタンパク質間相互作用(PPI: protein-protein interaction)を生じることで、有機低分子には不可能な機能を発現します。
環状ペプチドの特性は、アンメット・メディカル・ニーズを満たしてくれる医薬品としての可能性を秘めています。
更に、天然型のL-アミノ酸に限らず、非天然型D-アミノ酸やアミノ酸の修飾体などの「特殊アミノ酸」から「特殊ペプチド」を合成できれば、その構造に多様性が加わり、標的分子に対する特異性や体内動態の向上など可能性はより広がります。
6.フレキシザイムの登場
東京大学の菅教授らが開発した「フレキシザイム」という人工RNA触媒(リボザイム)が、ペプチド創薬の機運を高めることになります。
生体においてペプチドは、DNAが持つ遺伝情報が、まずmRNA(メッセンジャーRNA)に転写され、それに基づいてリボソームがアミノ酸を繋ぎ合わせてペプチドを合成します。mRNAの遺伝情報からペプチドが作られる過程は「翻訳」と呼ばれ、リボソームにアミノ酸を運ぶ役割を担うのが、tRNA(トランスファーRNA)です。tRNAは特定アミノ酸を自身に結合(アシル化)して運びますが、フレキシザイムは、特殊アミノ酸も含む任意のアミノ酸とtRNAを結合(アシル化)することができます1)。
この技術によって、1本の試験官中に、医薬品候補の可能性がある膨大な数の「特殊ペプチド」を1度に合成できるようになりました。この技術を基に、特殊ペプチドを応用した医薬品の研究開発を行う、東京大学発のバイオベンチャー「ペプチドリーム社」が2006年に設立されました。
7.新しいペプチド医薬品
世界中で多大な影響を与え続けている、近年の新型コロナウイルス問題。
SARS-CoV-2の感染が報告されて以来、ワクチンや中和抗体が開発、承認され、私たちをコロナから守ってくれています。現在も、国産ワクチンや有機低分子の抗ウイルス薬の開発が日本国内で進められています。
この中に、ペプチドリーム社が創製した特殊環状ペプチド「PA-001」も含まれています。
PA-001は、ウイルスの変異があまり起きていないスパイクタンパクS2領域を標的とする独自性の高い作用機序で、変異株に対しても有効性が確認されています。
また、経口投与でも高い血中濃度を維持できる可能性を動物試験で検証し、注射剤に次いで経口剤の開発も行われています2)。
近い将来、ペプチド医薬品だからこそ成しえた「新型コロナウイルス感染症治療薬」が登場する予定です。
(日本アイアール株式会社 特許調査部 K・H)
≪引用文献、参考文献≫
- 1)Curr Opin Chem Biol., 2007, 11(5), 537-542.
- 2)ペプチドリーム株式会社 プレスリリース
https://contents.xj-storage.jp/xcontents/45870/bf89ceaf/8e03/43a5/bee1/dbe8d7f8862f/20220204184149651s.pdf











](https://engineer-education.com/wp/wp-content/uploads/2024/01/solubilizer-150x150.png)




























