3分でわかる技術の超キホン 有機化合物の導電性の仕組み

導電性のものと聞いて、多くの方がまず頭に浮かぶのは、金、銀、銅、鉄などの金属でしょう。
炭素を含む化合物の大部分が有機物ということもあり、有機物は導電しないというイメージを持つ人は多いかもしれません。
しかし近年、有機EL、有機半導体、有機デバイスなどの言葉を頻繁に耳にするようになりました。
ここ数十年間、有機分子からなる分子ワイヤー、分子スイッチ等の分子エレクトロニクスの研究が盛んに行われ、導電性高分子をはじめ、単分子デバイスなどの有機素子が多く創り出されています。
そこで、今回は有機化合物の導電性の仕組みをご紹介します。
1.電子状態と共有結合
炭素原子が共有結合で結びついた化合物の多くは「有機化合物」です。
その導電性を説明する前に、電子状態と共有結合の説明を先にします。
原子にはもともと原子軌道がありますが、化学結合を形成する際に結合を結びやすいように、新たな原子軌道を作ることがあります。これを「混成軌道」と言います。
よく知られる炭素は、sp3、sp2、spと呼ばれる3種類の混成軌道を形成します。
また、原子2つの最外殻電子を1つずつ共有し合って形成した結合は「共有結合」と呼ばれ、σ結合とπ結合の二種類があります。
例えば、結合軸方向を向いた原子軌道同士による結合はσ結合であり、S軌道同士、S-P軌道、SPn混成軌道同士などの結合が含まれます。
π結合は、分子内の隣り合った原子同士の電子軌道のローブの重なりによってできる化学結合であり、σ結合より結合がは弱く、エネルギー準位は高いです。σ結合上の電子はσ電子と、π結合上の電子はπ電子と呼ばれます。σ電子は分子の骨格を作る電子で、π電子は動きやすい電子です。
今回は、有機分子の導電性の仕組みの説明なので、π電子について見てみましょう。

[図1.σ結合とπ結合]
2.ベンゼンの表示と非局在化π電子
π電子の動きによる非局在化で最も有名な分子は、「ベンゼン」でしょう。
ベンゼンは、6個の炭素原子がsp2混成軌道をとって六角平面上に配置しています。
Pz軌道にある6個のπ電子は非局在化しているため、環の上下に環状のπ電子雲を形成します。
ケクレ構造式では交代する二重結合と単結合で表されていますが、実際にはπ電子は特定の結合に寄与していないので、ベンゼン環を六角形の中に丸を書いた形で表示することがあります。
ベンゼン環を含む、安定した化合物を「芳香族化合物」と呼びます。
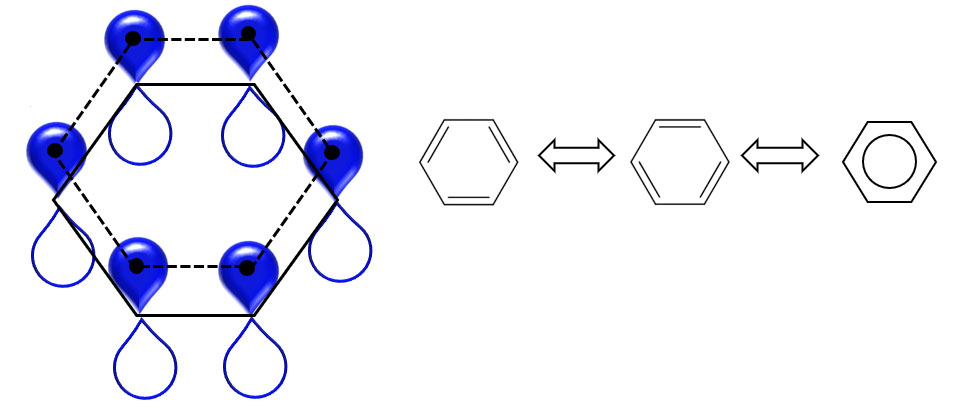
[図2.ベンゼンの表示と非局在化π電子]
3.π共役系と導電
ベンゼンと同じように、化合物中に交互に位置する単結合と多重結合に非局在化電子を持つ結合π軌道系は「π共役系」と呼ばれます。
2000年に白川英樹先生が、π共役高分子のひとつとしてポリアセチレンのドーピングによって共役高分子が金属のように電気をよく流すことを発見し、A.J. ヒーガー氏、A.G. マクアダイアミッド氏と共にノーベル化学賞を受賞されました。
ポリアセチレン自身はあまり電気は流れませんが、臭素やヨウ素の酸化剤を加えると、π電子の一部が引き抜かれて部分的にプラス(正孔)ができます(ドーピング過程)。
そのプラスを埋めるために隣のπ電子が動き、またその電子が抜けた場所にプラスができます。それが繰り返されることで電子が次々と動いて、金属と同じくらい電気を通すようになるのです。
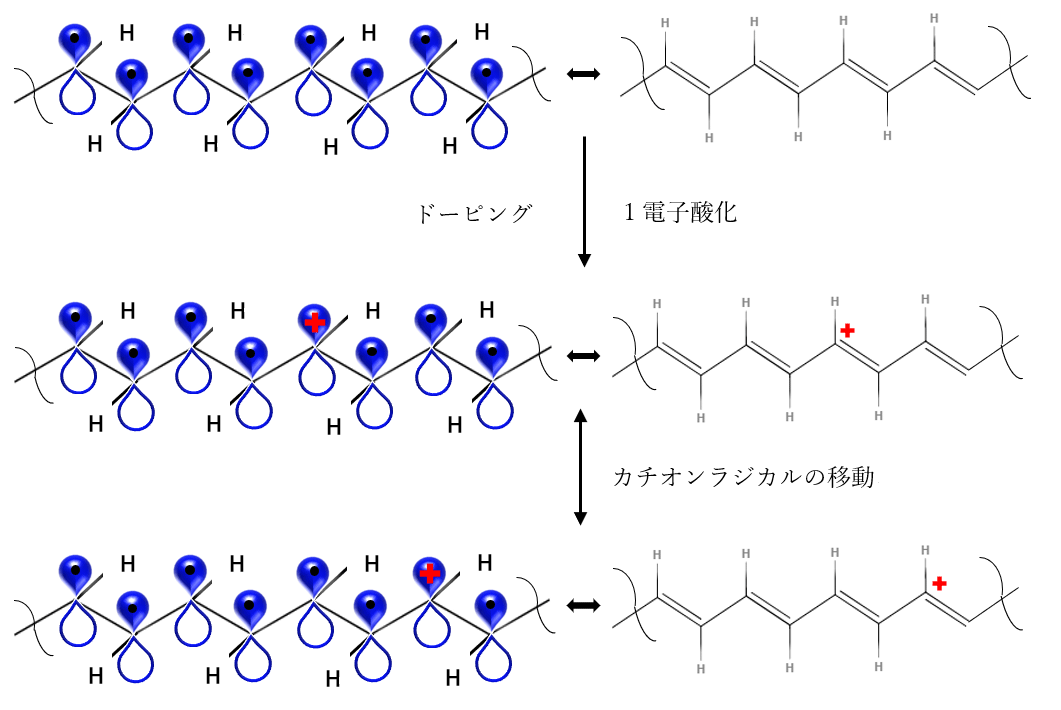
現在、様々な形を有するπ共役系が創り出され、有機半導体や有機単分子素子、有機デバイスなどの有機エレクトロニクスが盛んに研究されています。
実用化にはまだ様々な課題が残されていますが、その技術発展には大きな期待が寄せられています。
(日本アイアール株式会社 特許調査部 H・L)