ナノカーボンの製法が変わる?常温(室温)での合成に注目

1985年にフラーレンC60の発見が報告1)されてから40年近くになります。
フラーレンやカーボンナノチューブ(CNT)等の「ナノカーボン」の研究開発は現在も進行中です。
このナノカーボンの合成で近年大きな進展がありました。
1.ナノカーボンの製法|ナノカーボンの合成と温度
ナノカーボンは、通常、原料であるグラファイト等の炭素を超高温の状態に置いて炭素原子をいったん溶融か気化させた上で、これが凝縮する過程で準安定状態であるフラーレン等のナノカーボンを得る製法で合成されています。
具体的には、二つの黒鉛電極間でのアーク放電等が挙げられます。
図1に代表的なナノカーボンの構造を示します。
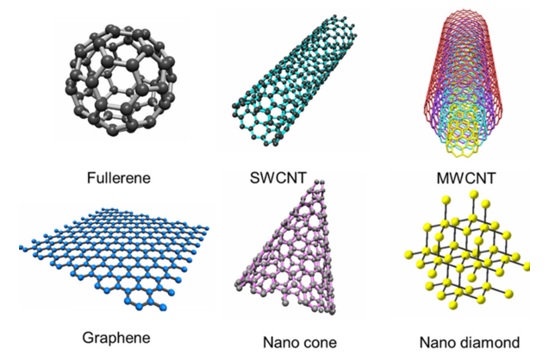
【図1 代表的なナノカーボン ※引用2)】
ナノカーボンの生成機構にはまだ不明な点が多いのですが、合成過程でC2分子(炭素2原子のみからなる分子)の存在が確認されています3)。
このC2分子は超高温の過酷条件(3,500℃以上の炭素蒸気中)でしか発生しないと考えられてきました。
つまりナノカーボンは超高温と密接につながった材料でした。
2.C2分子とは?
C2分子は二原子炭素(Diatomic Carbon)であって、分子量24.0であり12070-15-4というCASの登録番号を有する化学種です。当然ながらアセチレンC2H2とは別ものです。
他物質とは異なり、その物性を把握できるだけの十分な報告データがないのが実情です4)。
3.常温でのナノカーボン生成(東大・信州大・理研による報告)
C2分子は超高温でのみ存在するものと考えられていましたが、2020年に東京大学大学院薬学系の内山教授・宮本准教授らのチームが、図2に示すように、室温でのC2分子の合成とそれに引き続くナノカーボンの生成を報告しました5)。超高温での物理的な分解ではなく化学反応を用いての、しかも常温での処理です。
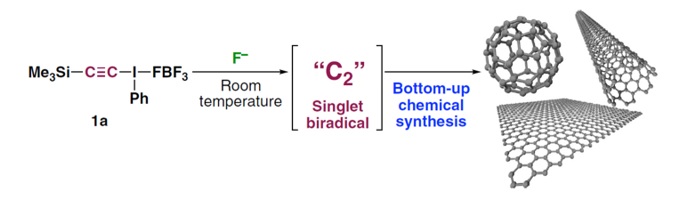
【図2 室温でのC2分子合成とナノカーボンの生成 ※引用5)】
C2分子の室温合成に成功した鍵は化合物1aにあります。
化合物1aは二つの異なる置換基を有するアセチレン誘導体です。
置換基の一つのI(Ph)FBF3はスーパー高速脱離基です。「超強力脱離基」と呼ばれれているトリフレートOSO2CF3の106倍もの脱離速度を持ちます。
このため、図3に示すように、F–によってMe3Si基が外れて化合物11が生成すると、化合物11から瞬時にI(Ph)FBF3が脱離してC2分子が生成したものと考えられます。
また、この報告から、ナノカーボンがC2分子から室温でも生成することも明らかになりました。
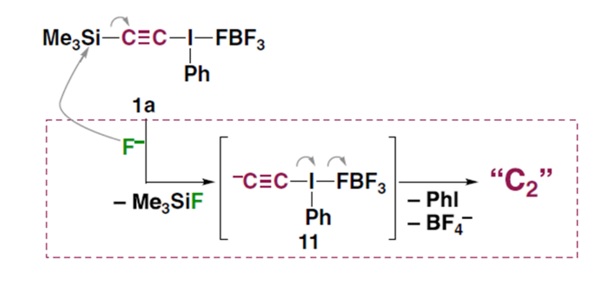
【図3 室温でのC2分子合成反応の機構】
フラーレンやカーボンナノチューブは従来法で商業生産されていますが、常温での合成成功は今後の生産法や用途展開に大きく影響する可能性があります。
(日本アイアール株式会社 特許調査部 N・A)
《引用文献、参考文献》
- 1) H. W. Kroto etc., C60: Buckminsterfulleren, Nature 318, 162–163 (1985)
- 2) Dang Sheng Su etc., Nanocarbons for the Development of Advanced Catalysts, Chem. Rev., 113(8), 5782–5816(2013)
- 3) 例えば、
鈴木信三, フラーレン・カーボンナノチューブの生成過程, ぶんせき2004(4), 193-198
https://www.jsac.or.jp/bunseki/pdf/bunseki2004/tenbo200404.PDF - 4) 米国国立生物工学情報センター(WEBサイト)
https://pubchem.ncbi.nlm.nih.gov/compound/Diatomic-carbon - 5) Kazunori Miyamoto etc., Room-temperature chemical synthesis of C2, NATURE COMMUNICATIONS 11:2134(2020)
https://www.nature.com/articles/s41467-020-16025-x