示差熱分析(DTA)の基礎知識:DTA曲線の読み方、測定・解析の注意点もわかる!

製品の品質保証や材料開発において、「熱的な挙動を正確に知ること」は非常に重要です。熱分析法の中でも、古くから広く用いられてきたのが「示差熱分析」(DTA)です。
本記事では、示差熱分析(DTA)の基本原理、装置構成から、基準物質やDTA曲線(グラフ)の読み解き方、さらには代表的な熱分析法である示差走査熱量測定(DSC)との違いまで、DTAに関する基礎知識をわかりやすく解説します。
目次
1.示差熱分析(DTA)とは?
「示差熱分析」(Differential Thermal Analysis:DTA)は、試料と基準物質を加熱・冷却しながら、その間に生じる温度差(ΔT)を測定する熱分析手法です。
試料に物理的または化学的な変化(例えば、融解、結晶化、酸化反応など)が起こると、エネルギーの吸収または放出が発生し、それにより温度差が生じます。DTAはこの温度差を追跡することで、材料の熱的挙動を把握します。
この手法は、セラミックス、金属、有機材料、医薬品、鉱物など、あらゆる固体・粉末材料の研究や品質管理に用いられており、現在も重要な熱分析技術の一つです。
[※関連記事:熱分析の種類と各種法の原理・特徴は? ]
《前提知識》物理的変化・化学的変化の現象と熱変化の関係
DTAの前提知識として、まず現象と熱変化の関係を説明します。
ご存じのように、私たちの身の回りには、加熱すると変化する物質が色々とあります。氷が水に溶ける、プラスチックが柔らかくなる、紙が燃えるなどの現象は、物理や化学変化に伴って、熱が吸収したり放出したりします。
物理的・化学的変化の現象と熱変化の関係を表1にまとめました。
| 現象 | 熱変化 | DTAでの表現 | |
| 化学的変化 | 分解反応 | 吸熱/発熱 | 吸熱/発熱ピーク |
| 酸化反応 | 発熱 | 発熱ピーク | |
| 燃焼 | 発熱 | 大きな発熱ピーク | |
| ポリマーの架橋反応 | 発熱 | 発熱ピーク | |
| 物理的変化 | 熔解 | 吸熱 | 吸熱ピーク |
| 昇華 | 吸熱 | 吸熱ピーク | |
| 結晶化 | 発熱 | 発熱ピーク | |
| ガラス転移 | 非熱容量が増大 | ベースラインのずれ、 吸熱ピークを伴うことが多い |
【表1 物理・化学変化の現象と熱変化の関係】
「物理変化」と「化学変化」の違いは質量の変化にあります。熱重量(TG)分析と連用すると、より多くの情報が入手できます。
例えば「ガラス転移」は、非晶質材料が硬いガラスのような状態から、ゴムのような可塑性状態へと変化することです。ガラス転移するとき、吸熱ではなく、比熱容量が急激に増大します。そのため、吸熱ピークではなく、ベースラインのずれが観察されます。
また、エンタルピー緩和*1)により、ガラス転移と同時に吸熱ピークが見られることもありますが、それは吸熱反応ではありません。
*1)エンタルピー緩和: ガラス状態の材料が、より安定な状態に移行する過程です。この緩和の過程で、熱が吸収されるため、ガラス転移温度付近で吸熱ピークとして現れることがあります。
2.DTAの原理
DTAの原理は次のようにシンプルなものです。
- 試料と基準物質(リファレンス)を同一環境下に配置する。
- 同じ速度で加熱または冷却する。
- その際に、試料側で吸熱・発熱反応が起こると、基準物質との間に温度差が生じる。
- この温度差(ΔT)を熱電対で検出し、時間または温度に対してプロットしたものが「DTA曲線」となる。
通常、基準物質は熱的に安定で、同じ加熱条件下で何も反応しないものが選ばれます。例えば、アルミナ(Al₂O₃)などがよく使われます。
3.DTA装置の構成
示差熱分析(DTA)装置は、材料の熱反応を測定するために、いくつかの基本的な要素で構成されています。
それぞれの役割を簡単に紹介します(図1)。
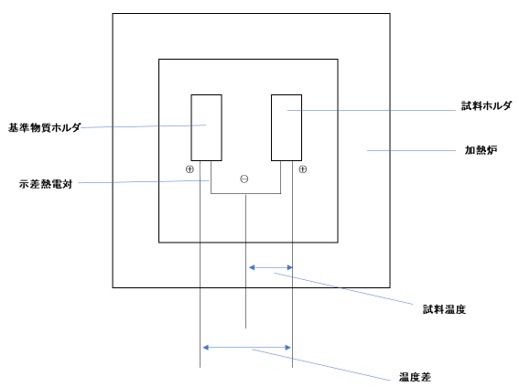
【図1 DTA装置の構成】
- 加熱炉(ヒーター):
試料と基準物質を一定の速度で加熱または冷却する部分です。内部の温度を均一に保つ構造になっており、加熱範囲は一般に室温から1000℃以上に対応します。酸素や窒素などの雰囲気ガスを流すことも可能です。 - 試料ホルダーと基準ホルダー:
加熱炉内には試料と基準物質を載せる専用の容器(ホルダー)があります。通常、アルミナや白金製であり、高温でも変形しにくく熱伝導性が安定しています。試料と基準物質はできるだけ同じ条件で配置されます。 - 熱電対(温度センサー):
試料と基準の温度差(ΔT)を高感度で検出するセンサーです。2本の熱電対が温度差を測り、その変化がDTA曲線に反映されます。
[※関連記事:温度センサ・温度測定技術の主な種類と基本原理がわかる! ] - 温度制御ユニット:
装置全体の加熱スケジュールを管理するシステムです。加熱速度や最終温度、保持時間などを自由に設定できます。安定した加熱が精度に直結します。 - データ処理ソフト・記録装置:
温度差のデータをリアルタイムで記録し、DTA曲線(グラフ)を作成するソフトウェアです。ピークの位置や大きさを自動で解析できる機能が付いています。
このように、DTA装置はシンプルな構造ながら、熱的な変化を正確にとらえるための工夫が詰まっています。
測定精度を高めるためには、ホルダーの選定や雰囲気ガスの制御、加熱条件の設定などが重要となります。
4.DTA曲線(グラフ)の読み方
「DTA曲線」(グラフ)は、材料の熱的変化を可視化したものです。
DTAの測定結果は、温度または時間を横軸(X軸)に、温度差(ΔT)を縦軸(Y軸)に取った二次元のグラフとして出力されます。このグラフの形状やピークから、どの温度で何が起こっているのかを把握できます。
以下に、DTA曲線の具体的な読み方について、段階を追って詳しく解説します。
(1)曲線の基本構造とゼロライン
DTA曲線の中心には、基準物質との温度差がない状態(ΔT = 0)を示す「ゼロライン」があります。
試料が何の熱変化も示していないとき、曲線はゼロライン上にあり、試料が反応すると曲線がゼロラインから上下方向に偏移します。この偏移が、熱的変化(吸熱 or 発熱)が発生した証拠です。
(2)吸熱ピークと発熱ピークの違い
DTA曲線には主に2種類のピークが現れます。
- 吸熱ピーク(Endothermic):
一般的に下向きのピーク(装置によっては逆の場合もあります)で、試料が熱を吸収する現象に対応します。
(代表例: 融解、脱水反応、熱分解) - 発熱ピーク(Exothermic):
上向きのピークであり、試料が熱を放出する現象に対応します。
(代表例: 結晶化、酸化反応)
なお、吸熱・発熱の表示方向は、装置の設定やメーカーによって異なる場合がある点に注意しましょう。
解析時は、ゼロラインの上下を基準に読み方を確認しましょう。
図2は試料と基準物質との温度差(ΔT)を時間tに対して描いたDTA曲線です。
加熱炉の昇温が始まると、試料、基準物質ともそれぞれの熱容量によって温度上昇を開始します。一般的に基準物質側より試料の熱容量が大きいことから、試料温度の上昇が遅れているため、①の斜線が観測されます。定常状態になると、試料と基準物質の熱容量の差も一定の量となり、この定常状態の信号を②のベースラインといいます。
さらに温度が上がると、③の吸熱ピークが出始めます。試料に融解などの吸熱反応が起こることを示唆します。融解が終わると急速に元のベースラインに戻り、吸熱ピーク③が検出されます。
また、発熱に伴う温度差をプラス方向に向けます。例えばその後、燃焼反応が起こると、ピーク④が現れます(図2)。
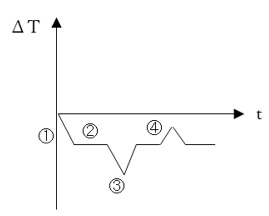
【図2 温度差の時間変化のDTA曲線】
(3)ピークの特徴量とその意味
DTA曲線の各ピークには、熱変化に関する重要な情報が含まれています。
| 特徴量 | 説明 | 意味 |
| ピーク開始温度(Tonset) | 曲線がベースラインから離れ始める温度 | 熱的変化の開始温度 |
| ピーク温度(Tmax) | ピークの最高点(吸熱なら最深点) | 反応が最も活発な温度 |
| ピーク終端温度(Tend) | 曲線が再びベースラインに戻る温度 | 熱的変化の終了温度 |
| ピーク面積(ΔA) | ピークの大きさ(ベースラインと曲線に挟まれた領域) | 熱変化の程度(定量評価は困難) |
【表2 ピークの特徴量とその意味】
(4)複数ピークの読み取りと反応の識別
DTAでは、1つの試料中に複数のピークが現れることがあります。
それぞれのピークは異なる熱イベントを表している可能性があります。
- 小さな吸熱ピーク ⇒ ガラス転移や水分の蒸発
- 鋭い吸熱ピーク ⇒ 融解や昇華
- 幅広い発熱ピーク ⇒ 結晶化や酸化反応(段階的に進行する)
ピーク同士の重なりやピーク間隔がある場合は、複数の相変化や反応が連続して起こっている可能性を示します。
(5)グラフ解釈時の注意点
DTA曲線を正確に読み解くには、以下の点に注意する必要があります。
- 雰囲気ガスの影響:
酸素雰囲気では酸化反応が強調されて発熱ピークが顕著になります。また、不活性雰囲気では、分解や相転移のみに集中します。 - 加熱速度の影響:
加熱速度が速いとピーク温度が高めにずれます。また、同じ試料でも加熱条件によりグラフが変化します。 - 基準物質との伝熱差:
不適切な基準物質を選ぶとピーク形状が歪んだりして、本来の反応が検出できなくなります。 - 機器のベースラインドリフト:
温度センサーの経年劣化や炉の構造によってベースラインが不安定になることがあるため、定期的なキャリブレーションが必要です。
(6)定性評価と定量評価の違い
DTAは主に定性分析に適した手法です。
- 定性評価: 熱的変化の有無、種類、発生温度の推定
- 定量評価: ピーク面積から熱量(エンタルピー)を求める。定量評価には、後述する示差走査熱量測定(DSC)の方が向いています。
5.DTAの用途
DTA曲線は、材料の熱的性質や反応挙動の「指紋」とも言える情報を提供してくれます。
特に、以下のようなケースにおいて、非常に有効となります。
- 未知物質の初期スクリーニング
- 材料の安定性比較
- 熱反応開始点の決定
- 工程条件の最適化(焼結温度や処理条件の決定)
DTAグラフを正しく読み解くことは、材料の理解を深める鍵となるのです。
6.DTAで使用される基準物質
基準物質はDTAにおいて重要な役割を果たします。
理想的な基準物質は次の条件を満たしている必要があります。
- 熱安定性が高い(加熱中に反応しない)
- 熱容量が一定
- 試料と似た熱伝導性を持つ
代表的な基準物質には、次のようなものがあります:
- アルミナ(Al₂O₃): セラミックス試料によく用いられる。
- シリカ(SiO₂): 高温安定性が高く、化学的にも安定。
- 酸化マグネシウム(MgO): 高温域での測定に適している。
基準物質の選択は、測定の信頼性や再現性に大きく影響するため、試料の特性に合わせて慎重に選ぶ必要があります。
7.示差走査熱量測定(DSC)との違い
DTAとよく比較されるのが、「示差走査熱量測定」(Differential Scanning Calorimetry:DSC)です。
両者の違いを簡単にまとめると以下の通りです(表3)。
| DTA | DSC | |
| 測定原理 | 温度差を測定(ΔT) | 熱量の差(ΔQ)を直接測定 |
| 定量性 | 熱量の定量は難しい | 熱量の定量が可能 |
| 感度 | やや劣る | 高感度 |
| 装置の構造 | 比較的シンプル | 精密かつ高価な装置が多い |
| 用途 | 熱的変化の有無を調べる | 熱量の定量と正確な熱イベント分析 |
【表3 DTAとDSCの比較】
DTAは「変化の検出」が主眼であり、DSCは「変化の定量」が強みです。用途や目的に応じて使い分けることが大切です。
8.DTAの欠点と限界
DTAには多くのメリットがありますが、以下のようなデメリットや限界も存在します。
- 定量性に乏しい: ピーク面積から熱量を求めるには複雑な補正が必要。
- 基準物質の影響を受けやすい: 選定ミスによって測定誤差が大きくなる。
- 微細な変化を検出しにくい: 感度はDSCに劣るため、微量な相変化には不向き。
- 測定条件に依存: 加熱速度や雰囲気ガスによって結果が変化する。
そのため、DTA単独での判断ではなく他の分析法との組み合わせや複数の測定条件での検証が推奨されます。
9.まとめ:DTAを活用して材料の熱特性を理解する
示差熱分析(DTA)は、材料の熱的特性や反応挙動を調べるための基本的かつ有効な手法です。
試料と基準物質の温度差を測定することで、相転移、分解、反応温度などを定性的に把握することができ、特に研究開発や品質管理において材料の熱挙動を理解する目的で多く活用されています。
DTAに興味をお持ちの方や、実務での応用に課題を感じている方には、熱分析に関する技術セミナーの受講をおすすめします。当サイトでは、DTAの初心者から中級者まで幅広く学べる講座をご紹介しています。ぜひご自身のレベル・目的に沿った講座をご検討ください。
(日本アイアール株式会社 特許調査部 H・L)
《引用文献、参考文献》
- 1)金網 久明, 「熱分析Ⅰ(DTA, DSC)」, 繊維と工業, Vol.3, No.10(1970), 670-676.








](https://engineer-education.com/wp/wp-content/uploads/2021/10/Circuit-element0-150x150.png)